
【题目】下列关于电离常数的说法正确的是( )
A.电离常数随着弱电解质的浓度增大而增大
B.CH3COOH的电离常数表达式为Ka= ![]()
C.CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小
D.电离常数只与温度有关,与浓度无关
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】对于反应放热反应A+B=C,下列条件的改变一定能使化学反应速率加快的是 ( )
A. 增加A的物质的量B. 升高体系温度C. 增加体系压强D. 降低体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1;
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJmol﹣1 .
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1:1
B.1:3
C.1:4
D.2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热方程式书写正确的是( )
A.2SO2+O2=2SO3△H=﹣196.6 kJ/mol
B.2H2(g)+O2(g)=2H2O(l)△H=﹣517.6 kJ/mol
C.H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.8 kJ
O2(g)=H2O(l)△H=﹣285.8 kJ
D.C(s)+O2(g)=CO2(g)△H=+393.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A.常温下,在 ![]() =1012的溶液中,Fe2+、I﹣、NO3﹣、Cl﹣一定不能大量共存
=1012的溶液中,Fe2+、I﹣、NO3﹣、Cl﹣一定不能大量共存
B.H2A是二元弱酸,常温下,0.1mol/LNaHA溶液的pH约为5,说明HA﹣电离程度大于水解程度
C.使用催化剂一定能够降低化学反应的反应热(△H)
D.NA为阿伏加德罗常数的值,常温常压下,28gC2H4和C3H6混合气体含有的原子数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】英国科学家道尔顿曾经说过:“有的人能够远远超越其他人,其主要原因与其说是天才,不如说他有专心致志坚持学习和不达目的决不罢休的顽强精神”,道尔顿为近代化学科学的发展作出的卓越贡献是( )
A. 提出元素的概念
B. 建立燃烧现象的氧化学说
C. 提出原子学说,为近代化学的发展奠定坚实的基础
D. 发现元素周期律,把化学元素及其化合物纳入一个统一的体系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃和101kPa时
①CO(g)+ ![]() O2(g)═CO2(g)△H1=﹣a kJ/mol
O2(g)═CO2(g)△H1=﹣a kJ/mol
②H2(g)+ ![]() O2(g)═H2O(l)△H2=﹣b kJ/mol
O2(g)═H2O(l)△H2=﹣b kJ/mol
③C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H3=﹣c kJ/mol
(1)试计算2CO(g)+4H2(g)═H2O(l)+C2H5OH(l)的△H= .
(2)对反应N2O4(g)2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法 不正确的是________
A.A、C两点的反应速率:A<C
B.B、C两点的气体的平均相对分子质量:B>C
C.A、C两点气体的颜色:A深,C浅
D.由状态A到状态B,可以用降温的方法
(3)在100℃时,将0.50mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如表数据:
时间(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.50 | n1 | 0.34 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.10 | 0.10 |
①上述条件下,前20秒二氧化氮的平均反应速率为 ,平衡时二氧化氮的转化率为 .
②该温度下,反应的平衡常数K值为 .(保留一位小数)
(4)甲醇﹣空气的燃料电池(电解质为KOH溶液)得到广泛应用,请写出该燃料电池负极的电极反应式 ,若通入空气之前电解质KOH溶液的浓度为0.6mol/L,体积为100mL,当电子转移0.15mol后电解质溶液的pH为 .(体积保持不变,室温条件)
(5)电离度指弱电解质在溶液里达电离平衡时,已电离的电解质分子数占原来总分子数的百分数.若室温下,c mol/L氨水的电离平衡常数为Kb , 则该氨水的电离度 α= .(请用c和Kb表示,可进行近似计算)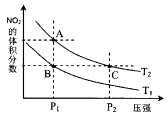
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是
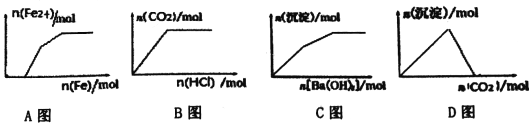
A. Fe(NO3)3、Cu(NO3)2、HNO3混合溶液中逐渐加入铁粉
B. Na2CO3、NaHCO3溶液中逐滴加入HCl
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液
D. NaAlO2溶液中逐渐通入CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( ) 
A.原子半径:W<X<Y
B.元素的非全属性:Z>Y>X
C.化合物XYZ中只含共价键
D.K、L、M中沸点最高的是M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com