


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、红棕色的NO2,加压后颜色先变深后变浅 |
| B、高压比常压有利于合成SO3的反应 |
| C、合成NH3在较高温度下进行 |
| D、黄绿色的氯水光照后颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑤ | B、②③④ |
| C、③④⑥ | D、⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| B、标准状况下,22.4 L NH3中含有共价键的数目为NA |
| C、1 molCl2与足量Fe反应转移电子数一定为3NA |
| D、标准状况下,11.2 L SO3所含的分子数目为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、92 g NO2和N204混合气体中含有的原子数为3NA |
| B、标准状况下,11.2 L H2O中含有的电子数为20NA |
| C、0.5mol?L“的Ba(0H)2溶液中0H一的数目为NA |
| D、1 mol Mg与足量的02或N2反应生成MgO或Mg3N2时,失去的电子数均为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应中的能量变化,通常表现为热量的变化 |
| B、煤和石油属于可再生能源 |
| C、要使燃料燃烧只需要大量的氧气 |
| D、汽车排出大量尾气中含有CO会污染大气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
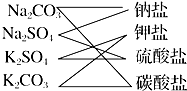 如图所示是对Na2CO3、Na2SO4、K2CO3、K2SO4四种物质进行的分类,这种分类方法的名称是( )
如图所示是对Na2CO3、Na2SO4、K2CO3、K2SO4四种物质进行的分类,这种分类方法的名称是( )| A、交叉分类法 | B、树状分类法 |
| C、圈图法 | D、链状箭头法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com