
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO与Cl2在常温常压下反应得到。ClNO部分性质如下:黄色气体,熔点:-59.6℃,沸点:-6.4℃,遇水易水解。已知:HNO2既有氧化性又有还原性;AgNO2微溶于水,能溶于硝酸:AgNO2+HNO3= AgNO3+ HNO2。
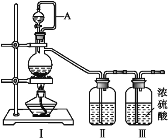
(1)利用Ⅰ、Ⅱ、Ⅲ装置制备原料气NO和Cl2
① 写出利用装置Ⅰ制备氯气的离子反应方程式:_________。
② 利用上述装置制备NO时,Ⅱ中盛装物质为_________(写化学式)。
(2)利用以下装置在常温常压下制备ClNO
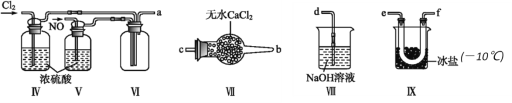
① 装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
② 为使NO和Cl2恰好完全反应生成ClNO,理论上通入NO和Cl2两种气体的流速比为_________。
③ 装置Ⅸ的作用是_____________。
④ 装置Ⅷ吸收尾气时,有同学认为尾气中的某种气体不能完全被吸收,为了充分吸收尾气,可将尾气与______________(气体)同时通入NaOH溶液中。
⑤ 王水是浓盐酸和浓硝酸的混酸,一定条件下混酸可生成ClNO和Cl2,该反应的化学方程式为______________________________________。
⑥ 写出验证ClNO与H2O完全反应后的溶液中存在Cl-和HNO2的实验步骤:取少量反应后的溶液于试管中,______________________________________________________。(限选试剂如下:AgNO3溶液,稀硝酸,KMnO4溶液)
【答案】MnO2+4H++2Cl-![]() Mn2+ + Cl2↑+2H2O H2O a→e→f→c→b→d (或a→f→e→c→b→d) 2∶1 冷凝亚硝酰氯,便于收集 O2(或空气) HNO3(浓)+3HCl(浓)=ClNO↑+Cl2↑+2H2O 依次滴加足量的AgNO3溶液和稀硝酸,充分振荡、静置,有白色沉淀生成;另取静置后上层清液少许于另一支试管中,滴加KMnO4溶液,溶液紫色褪去
Mn2+ + Cl2↑+2H2O H2O a→e→f→c→b→d (或a→f→e→c→b→d) 2∶1 冷凝亚硝酰氯,便于收集 O2(或空气) HNO3(浓)+3HCl(浓)=ClNO↑+Cl2↑+2H2O 依次滴加足量的AgNO3溶液和稀硝酸,充分振荡、静置,有白色沉淀生成;另取静置后上层清液少许于另一支试管中,滴加KMnO4溶液,溶液紫色褪去
【解析】
(1)、①制备氯气的离子反应方程式:MnO2+4H++2Cl-![]() Mn2+ + Cl2↑+2H2O;
Mn2+ + Cl2↑+2H2O;
②实验室收集NO只能用排水法,选择试剂H2O;
(2)、①ClNO易与水反应,装置VII可以防止尾气吸收装置VIII的水蒸气进入,所以连接顺序为a→e→f→c→b→d;
②由反应2NO+Cl2=2ClNO可知理论上通入NO和Cl2两种气体的流速比为2:1时恰好完全反应生成ClNO;
③ 由于ClNO沸点:-6.4℃,所以需要冰盐(-10℃)冷凝亚硝酰氯,才便于收集;
④空气中氧气与NO反应生成NO2,同时通入NaOH溶液中被NaOH溶液吸收,避免NO逸出污染空气;
⑤王水是浓盐酸和浓硝酸的混酸,一定条件下混酸可生成ClNO和Cl2,根据得失电子守恒和原子守恒,该反应的化学方程式为:HNO3(浓)+3HCl(浓)=ClNO↑+Cl2↑+2H2O;
⑥验证ClNO与H2O完全反应后的溶液中存在Cl-和HNO2,可根据Cl-与Ag+反应生成白色沉淀及HNO2具有还原性进行判断,具体操作为:依次滴加足量的AgNO3溶液和稀硝酸,充分振荡、静置,有白色沉淀生成;另取静置后上层清液少许于另一支试管中,滴加KMnO4溶液,溶液紫色褪去。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子立体结构.其要点可以概括为:
Ⅰ、用AXnEm表示只含一个中心原子的分子,A为中心原子,X为与中心原子相结合的原子,E为中心原子最外层未参与成键的电子对(称为孤对电子),(n+m)称为价层电子对数.分子中的价层电子对总是互相排斥,均匀的分布在中心原子周围的空间;
Ⅱ、分子的立体构型是指分子中的原子在空间的排布,不包括中心原子未成键的孤对电子;
Ⅲ、分子中价层电子对之间的斥力的主要顺序为:
i、孤对电子之间的斥力>孤对电子对与共用电子对之间的斥力>共用电子对之间的斥力;
ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;
iii、X原子得电子能力越弱,A﹣X形成的共用电子对之间的斥力越强;
iv、其他.
请仔细阅读上述材料,回答下列问题:
(1)根据要点I可以画出AXnEm的VSEPR理想模型,请填写下表__:

(2)H2O分子的立体构型为:__,请你预测水分子中∠H﹣O﹣H的大小范围__;
(3)SO2Cl2和SO2F2都属AX4E0型分子,S=O之间以双键结合,S﹣Cl、S﹣F之间以单键结合.请你预测SO2Cl2和SO2F2分子的立体构型:__,SO2Cl2分子中∠Cl﹣S﹣Cl__(选填“<”、“>”或“=”)SO2F2分子中∠F﹣S﹣F。
(4)用价层电子对互斥理论(VSEPR)判断SO32﹣离子的空间构型:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式__________。
(2)已知在25℃、101kPa下,1 g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7 kJ的热量,试写出乙醇燃烧热的热化学方程式_______________。
(3)标准状况下,4.48L H2在足量O2中完全燃烧放出热量Q kJ,写出H2燃烧的热化学方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物的描述正确的是
A. 组成为C6H14的烷烃中仅能由1种单炔烃加氢而制得的结构有2种
B. 立方烷( ![]() )燃烧的现象与乙烷燃烧的现象相同
)燃烧的现象与乙烷燃烧的现象相同
C. ![]() 分子中所有原子不可能处于同一平面
分子中所有原子不可能处于同一平面
D. 用碳酸钠溶液不能一次性鉴别乙酸、苯和乙醇三种无色液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将等浓度等体积的弱酸HA和HB与NaHCO3反应放出CO2的体积与时间的关系如图所示,则以下说法错误的是:( )

A. 酸性:HA<HB
B. pH均为4的HA和HB溶液中和等量NaOH时,所需HA溶液体积小
C. pH均为9的NaA溶液和NaB溶液相比,NaA溶液中水的电离程度大
D. 浓度均为0.1mol/L的NaA溶液和NaB溶液相比,NaA溶液中水的电离程度大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种金属组成的合金25克与氯气完全反应,共用去标况下氯气11.2升,该合金的可能组成是
A.Na和MgB.Cu和CaC.Cu和ZnD.Fe和Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)![]() pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是
pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是

①m+n>p ②x点表示的正反应速率大于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若升高温度,该反应的平衡常数增大
A. ①②⑤ B. 只有②④ C. 只有①③ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种溶液分别是氢氧化钡溶液、氨水、醋酸溶液、盐酸中的一种。
已知同浓度的四种溶液:①加入大小完全相同的镁条,仅A、C中放出气体,且开始时A中冒气泡的速度快;②相同条件下,取B、D溶液进行导电性实验,发现导电能力最差的是D。回答下列问题:
(1)D溶液为_______________;同浓度的四种溶液中,pH值最大的是______________(填化学式)溶液。
(2)pH值和体积均相同的A和C溶液,分别与足量大小完全相同的锌粒反应,开始时的反应速率
v(A)______________v(C) (填“>”“<”或“=”)
(3)等体积等浓度的氨水和盐酸混合后,所得溶液呈______________(填“酸性”、“碱性”或“中性”),用离子方程式解释其原因__________________________________。
(4)常温下,2mol/L的NaOH溶液与amol/L的醋酸溶液等体积混合后,发现溶液呈中性,
试计算:该温度下醋酸钠的水解平衡常数Kb=________________(用含a的代数式表示。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列浓度关系正确的是( )
A. 0.1mol/L的NH4HSO4溶液中滴加0.1mol/L的Ba(OH)2溶液至沉淀刚好完全:c(NH4+)>c(OH-)>c(SO42-)>c(H+)
B. 若将CO2通入0.1mol/LNa2CO3溶液至溶液中性,则溶液中: 2c(CO32-)+c(HCO3-)=0.1mol/L
C. 0.1mol/L的NaOH溶液与0.2mol/L的HCN溶液等体积混合,所得溶液呈碱性:c(Na+)>c(CN-)>c(HCN)>c(OH-)>c(H+)
D. 向1L 1mol/L的KOH热溶液中通入一定量的Cl2,恰好完全反应生成氯酸钾、次氯酸钾和氯化钾的混合溶液:c(K+)+c(H+)=6c(ClO3-)+2c(ClO-)+c(HClO)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com