
| 物质 | △H(kJ?mol-1) | 物质 | △H(kJ?mol-1) |
| C(s) | -393.5 | C2H6(g) | -1559.8 |
| H2(g) | -285.8 | C3H8(g) | -2219.9 |
| C2H4(g) | -1411.0 | C12H26(l) | -8162.0 |
| 2219.9 |
| 393.5 |
| 1 |
| 2 |
| 7 |
| 2 |


科目:高中化学 来源:不详 题型:填空题
 ,HSO
,HSO 在较稀(如1 mol·L-1以下)的溶液中,可完全电离为H+和SO
在较稀(如1 mol·L-1以下)的溶液中,可完全电离为H+和SO 。不过,在浓度大的溶液中HSO
。不过,在浓度大的溶液中HSO 不能完全电离,而是与H+、SO
不能完全电离,而是与H+、SO 共同存在于同一溶液中。
共同存在于同一溶液中。| A.酸 | B.盐 | C.碱 | D.氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
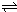 CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
CH3OH(g)进行过程中的能量变化曲线.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )| A.其它条件不变,按曲线b线进行的反应,CH3OH的产率更高 |
| B.其它条件不变,分别按曲线a、b线进行的反应的热效应相同 |
| C.(1molCO+2molH2)中的键能之和比1molCH3OH中的键能之和大 |
D.热化学方程式为CO(g)+2H2(g) CH3OH(g)△H=-91kJ?mol-1 CH3OH(g)△H=-91kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
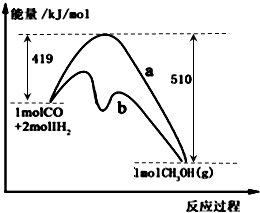
| A.2个H2分子和O2反应放出571.6kJ?mol-1的热量 |
| B.2molH2(g)完全反应生成2H2O(g),放出热量为571.6kJ |
| C.在298k时,2molH2(g)和1molO2(g)完全反应生成1molH2O(g)放出热量571.6kJ |
| D.在298k时,2molH2(g)和1molO2(g)完全反应生成1molH2O,放出热量571.6kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等质量的O2比O3能量低,由O2变为O3为放热反应 |
| B.O3比O2稳定,由O2变为O3为吸热反应 |
| C.O2比O3稳定,由O2变为O3为放热反应 |
| D.等质量的O2比O3能量低,由O2变为O3为吸热反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧化还原反应都是放热反应 |
| B.化学反应过程中一定有化学键的断裂和形成 |
| C.伴随能量变化的物质变化都是化学变化 |
| D.化学反应过程中,分子的种类和数目一定发生改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2molSO2(g)和1molO2(g)所具有的内能小于2molSO3(g)所具有的内能 |
| B.将2molSO2(g)、1molO2(g)置于一密闭容器中充分反应后放出QkJ的热量 |
| C.升高温度,平衡向正反应方向移动,上述热化学方程式中的Q值减小 |
| D.如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QkJ,则此过程中有2molSO2(g)被氧化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 xC(g)+D(g)中,已知:反应开始加入的物质只有A、B;起始浓度A为5 mol·L-1,B为3 mol·L-1,前2 min C的平均反应速率为0.5 mol·L-1·min-1。2 min后,测得D的浓度为0.5 mol·L-1。(设反应前后溶液体积不变)则关于此反应的下列说法中正确的是( )
xC(g)+D(g)中,已知:反应开始加入的物质只有A、B;起始浓度A为5 mol·L-1,B为3 mol·L-1,前2 min C的平均反应速率为0.5 mol·L-1·min-1。2 min后,测得D的浓度为0.5 mol·L-1。(设反应前后溶液体积不变)则关于此反应的下列说法中正确的是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com