
三硅酸镁被用来治疗胃酸过多的胃溃疡,是因为该物质不溶于水,服用后能中和胃酸,作用持久.把三硅酸镁 ·n
·n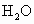 改写成氧化物的形式为________,它中和胃酸(HCl)的化学方程式是________.
改写成氧化物的形式为________,它中和胃酸(HCl)的化学方程式是________.
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源:2007-2008江苏省秋实学苑期中考试化学试卷 题型:022
胃酸过多是常见的胃病.下面是甲、乙两种常见胃药的说明摘要.
甲:①白色结晶状粉末,受热可缓缓分解;②能溶于水,水溶液呈弱碱性;灼烧时火焰为黄色;③遇酸及酸性药物则产生二氧化碳;④患者服用过量,可能引起胃胀气,甚至有引起胃溃疡穿孔的危险.
乙:①与胃酸是中和作用缓慢而持久,可维持3~4小时;②凝胶本身覆盖于溃疡面上,具有保护作用;③可溶于稀酸或氢氧化钠溶液中.
(1)请你推测,甲中含有的主要化学成份是________(填化学式);乙中含有的主要化学成份是________(填化学式).
(2)试写出甲中含有的主要化学成份引起胃胀气反应的离子方程式:________.
(3)三硅酸镁Mg2Si3O8·nH2O也是常用胃药,被用来治疗胃溃疡,是因为该物质不溶于水,服用后中和胃酸作用持久.把三硅酸镁改写成氧化物形式为:________.
写出它中和胃酸(胃酸的主要成分是HCl)的化学方程式________.
(4)目前一种新型抗酸剂能迅速改善和缓解胃酸过多的症状,它主要由碳酸镁、氢氧化镁和氢氧化铝组成(说明:Mg(OH)2在高温下分解为MgO).现按如下步骤测定药剂中三种主要成分的配比:
①取药剂样品,研磨后,加入50 mL 3.6 mol·L-1盐酸,正好完全反应并收集得到标准状况下224 mL气体
②过滤,弃去其中不溶性物质(其余成分不参与反应)
③取②中滤液,加入足量的NaOH溶液后,过滤、洗涤、灼烧,所得固体2.4 g.
则该药剂中三种主要成分的物质的量之比为n(MgCO3)∶n(Mg(OH)2)∶n(Al(OH)3)=________.
查看答案和解析>>
科目:高中化学 来源:期末题 题型:填空题
查看答案和解析>>
科目:高中化学 来源:0110 期中题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com