
| A. | NaOH溶液和CO2的反应 | B. | Ba(OH)2溶液和稀硫酸的反应 | ||
| C. | NaOH溶液和稀硫酸反应 | D. | 氨水和稀硫酸的反应 |
分析 离子方程式H++OH-═H2O表示可溶性强碱与强酸反应生成可溶性盐和水的一类反应,酸不能为弱酸,如:碳酸、醋酸等;碱不能为弱碱,如氨水,据此进行判断.
解答 解:A.二氧化碳不能拆开,氢氧化钠溶液过量时,该反应的离子方程式为:2OH-+CO2=CO32-+H2O,不能用H++OH-═H2O表示,故A错误;
B.氢氧化钡与稀硫酸反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不能用H++OH-═H2O表示,故B错误;
C.氢氧化钠与稀硫酸反应的离子方程式为:H++OH-═H2O,故C正确;
D.一水合氨为弱碱,离子方程式中一水合氨不能拆开,反应的离子方程式为:H++NH3•H2O=H2O+NH4+,其离子方程式不能用H++OH-═H2O表示,故D错误;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,明确离子方程式表示的意义为解答关键,注意熟练掌握离子方程式的书写原则,试题培养了学生的规范答题能力.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:解答题
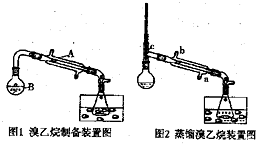 已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:| 溶解性(本身均做溶剂) | 沸点(℃) | 密度(g/mL) | |
| 水混溶,易溶于有机溶剂 | 78.5 | 0.8 | |
| 难溶于水,易溶于有机溶剂 | 38.4 | 1.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸并加热 | |
| B. | KNO3溶液(AgNO3):加过量KCl溶液,过滤 | |
| C. | NaCl溶液(Br2):加CCl4,分液 | |
| D. | NaCl溶液(KNO3):加热蒸发得浓溶液后,降温,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
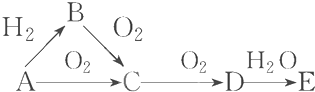
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
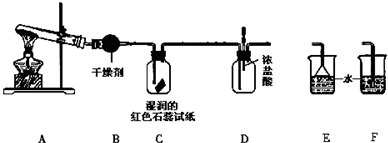
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将SO2通入酸性KMnO4溶液中 | 溶液紫红色褪去 | SO2具有漂白性 |
| B | 向某溶液中滴加盐酸 | 有气泡产生 | 该溶液一定含有CO32- |
| C | 将CO2通入Na2SiO3溶液中 | 产生白色胶状物质 | 证明H2CO3酸性比H2SiO3强 |
| D | 对某白色固体进行焰色反应实验 | 火焰呈黄色 | 该物质一定只含钠盐 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
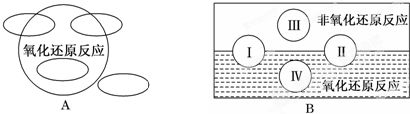
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com