
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入适量醋酸钠晶体后,两溶液的pH均增大 | |
| B. | 将温度升高至50℃,两溶液的pH均不变 | |
| C. | 加水稀释至原体积的2倍后,两溶液的pH均减小 | |
| D. | 加入足量锌粉充分反应后,两溶液产生氢气一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核内质子数为131 | B. | 核内中子数为131 | C. | 原子序数为53 | D. | 质量数为53 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
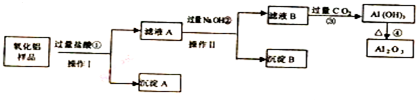
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用燃煤脱硫技术,防止SO2污染 | |
| B. | 采用绿色化学生产工艺,提高原子利用率 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加大石油、煤炭的开采力度,增加化石燃料的供应量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入铝粉放出H2的溶液中:Al3+、K+、SO42-、Cl- | |
| B. | 1.0 mol•L-1的KNO3溶液中:Na+、Fe2+、Cl-、SO42- | |
| C. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液中:K+、Cu2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化钠、氧化铁、氧化镁均为碱性氧化物 | |
| B. | 离子键、共价键、金属键、氢键均为化学键 | |
| C. | 氨水、水玻璃、水银、聚乙烯均为混合物 | |
| D. | 水能、风能、生物质能、核能均为可再生能源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com