
【题目】(1)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+![]() Cl2(g) ΔH1=83 kJ·mol 1
Cl2(g) ΔH1=83 kJ·mol 1
CuCl(s)+![]() O2(g)=CuO(s)+
O2(g)=CuO(s)+![]() Cl2(g) ΔH2= 20 kJ·mol 1
Cl2(g) ΔH2= 20 kJ·mol 1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3= 121 kJ·mol 1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=_________ kJ·mol 1。其中O2的电子式为__________
(2)硅粉与HCl在300℃时反应生成1mol SiHCl3气体和H2 ,放出225KJ热量,该反应的热化学方程式为________________________。SiHCl3中含有的化学键类型为__________
(3)将SiCl4氢化为SiHCl3有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g)![]() SiHCl3(g)+HCl(g) ΔH1>0
SiHCl3(g)+HCl(g) ΔH1>0
②3SiCl4(g)+2H2(g)+Si(s)![]() 4SiHCl3(g) ΔH2<0
4SiHCl3(g) ΔH2<0
③2SiCl4(g)+H2(g)+Si(s)+HCl(g)![]() 3SiHCl3(g) ΔH3
3SiHCl3(g) ΔH3
则反应③的ΔH3______(用ΔH1,ΔH2表示)。
(4)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得.请写出反应的离子方程式________________________
(5)氯化铵常用作焊接.如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:_______CuO+______NH4Cl![]() ______Cu+______CuCl2+______N2↑+______H2O
______Cu+______CuCl2+______N2↑+______H2O
①配平此氧化还原反应方程式___________________________
②此反应中若产生0.2mol的气体,则有__________mol的电子转移.
【答案】-116 ![]() Si(s)+3HCl(g)=SiHCl3(g)+H2(g) △H=-225kJ·mol-1 共价键 △H2-△H1 2ClO3-+SO32-+2H+=2ClO2↑+SO42-+H2O 4CuO+2NH4Cl
Si(s)+3HCl(g)=SiHCl3(g)+H2(g) △H=-225kJ·mol-1 共价键 △H2-△H1 2ClO3-+SO32-+2H+=2ClO2↑+SO42-+H2O 4CuO+2NH4Cl![]() 3Cu+CuCl2+N2↑+4H2O 1.2
3Cu+CuCl2+N2↑+4H2O 1.2
【解析】
(1)①CuCl2(s)=CuCl(s)+![]() Cl2(g),②CuCl(s)+
Cl2(g),②CuCl(s)+![]() O2(g)=CuO(s)+
O2(g)=CuO(s)+![]() Cl2(g),③CuO(s)+2HCl(g)=CuCl2(s)+H2O(g),根据目标反应方程式,2×①+2×②+2×③得出2×(△H1+△H2+△H3)=2×(83-20-121)kJ·mol-1=-116kJ·mol-1;O2分子中有共价键,其电子式为
Cl2(g),③CuO(s)+2HCl(g)=CuCl2(s)+H2O(g),根据目标反应方程式,2×①+2×②+2×③得出2×(△H1+△H2+△H3)=2×(83-20-121)kJ·mol-1=-116kJ·mol-1;O2分子中有共价键,其电子式为![]() ;
;
(2)硅粉与HCl反应的方程式为Si+3HCl=SiHCl3+H2,生成1molSiHCl3,放出225kJ,因此热化学反应方程式为Si(s)+3HCl(g)=SiHCl3(g)+H2(g) △H=-225kJ·mol-1;SiHCl3属于共价化合物,含有共价键;
(3)根据盖斯定律,推出②-①得出△H3=△H2-△H1;
(4)根据信息,KClO3被还原成ClO2,SO32-被氧化成SO42-,根据化合价升降法进行配平,其离子方程式为2ClO3-+SO32-+2H+=2ClO2↑+SO42-+H2O;
(5)①根据化合价升降法进行配平,得出4CuO+2NH4Cl![]() 3Cu+CuCl2+N2↑+4H2O;
3Cu+CuCl2+N2↑+4H2O;
②根据反应方程式,生成1molN2,转移电子物质的量为6mol,即生成0.2molN2时,转移电子物质的量为0.2mol×6=1.2mol。


科目:高中化学 来源: 题型:
【题目】一定量的Cu粉与浓H2SO4共热产生SO2气体的体积为2.24 L(标准状况下),则下列情况不可能的是( )
A.加入Cu的质量为6.4 g
B.加入的浓H2SO4中含溶质0.2 mol
C.加入Cu的质量大于6.4 g
D.加入浓H2SO4中含溶质多于0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物J 是我国自主成功研发的一类新药,它属于酯类,分子中除苯环外还含有一个五元环。合成J的一种路线如下:
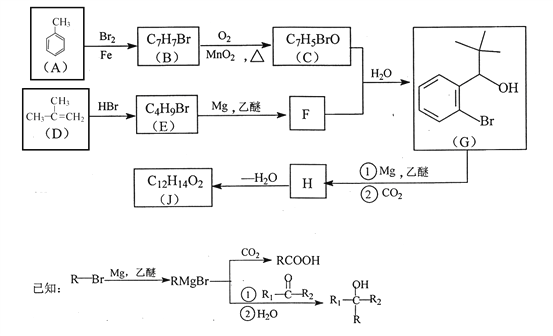
回答下列问题:
(1)B的结构简式是________________。C的结构简式是______________。
(2)D生成 E的化学方程式为_________________。
(3)J的结构简式是________________。在一定条件下,H自身缩聚生成高分子化合物的结构简式是_______________。
(4)根据![]() ,X的分子式为______。X有多种同分异构体,其中满足下列条件的同分异构体共有______种(已知:碳碳叁键或碳碳双键不能与羟基直接相连)。
,X的分子式为______。X有多种同分异构体,其中满足下列条件的同分异构体共有______种(已知:碳碳叁键或碳碳双键不能与羟基直接相连)。
A.除苯环外无其他环,且无一O—O—键
B.能与FeCl3溶液发生显色反应
C.苯环上一氯代物只有两种
(5)利用题中信息和所学知识,写出以甲烷和甲苯 为原料,合成![]() 的路线流程图(其它试剂自选):____________________________。
的路线流程图(其它试剂自选):____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3DZn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3DZn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。
ZnO(s)+2Ni(OH)2(s)。

A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B. 充电时阳极反应为Ni(OH)2(s)+OH(aq)e![]() NiOOH(s)+H2O(l)
NiOOH(s)+H2O(l)
C. 放电时负极反应为Zn(s)+2OH(aq)2e![]() ZnO(s)+H2O(l)
ZnO(s)+H2O(l)
D. 放电过程中OH通过隔膜从负极区移向正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氯甲烷与苯的反应如图所示(无机小分子产物略去)。下列说法正确的是
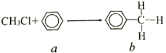
A.该反应属于化合反应
B.a与溴水在铁作催化剂条件下反应生成溴苯
C.b中最多有14个原子共平面
D.b的二氯代物有10种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠是一种防腐剂和增色剂,但在食品中过量时会对人体产生危害,其在酸性条件下会产生NO和NO2。下列有关说法错误的是
A. NaNO2既可以使酸性高锰酸钾溶液褪色,又可以将二价铁离子氧化为三价铁离子
B. 食用“醋熘豆芽”可能会减少亚硝酸钠对人体的危害
C. NaNO2和胃酸作用的离子方程式为2NO2-+2H+![]() NO↑+NO2↑+H2O
NO↑+NO2↑+H2O
D. 1 mol NaNO2在酸性条件下完全反应生成NO和NO2,转移电子的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 在一定条件下,可逆反应A+B![]() mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况。
mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况。

(1)温度T1________T2(填“大于”“等于”或“小于”)。
(2)正反应是________反应(填“吸热”或“放热”)。
(3)如果A、B、C均为气体,则m________2(填“大于”“等于”或“小于”)。
(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强________(填“增大”“减小”或“不变”),平衡_________________移动(填“向正反应方向”“向逆反应方向”或“不”)。
II. CO是生产羰基化学品的基本原料, 850℃时,在恒容密闭容器中通入CO和H2O(g),发生:CO(g)+H2O(g) ![]() H2(g)+CO2(g)
H2(g)+CO2(g) ![]() H<0,测定浓度随时间关系如下表:
H<0,测定浓度随时间关系如下表:
t/min | c(CO)/ mol·L-1 | c(H2O)/ mol·L-1 |
0 | 0.30 | 0.20 |
2 | \ | 0.10 |
3 | 0.18 | \ |
4 | \ | 0.08 |
回答下列问题
(1)t=3min时,υ(正)____________υ(逆)(选填:“>”,“<”,“=”)。
(2)0~2min,CO的平均反应速率为 ____________。
(3)上述反应中的CO平衡转化率为____________。
(4)在一定条件下,发生下列反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示,则t1时改变的某种反应条件可能是_____(填序号)。
H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示,则t1时改变的某种反应条件可能是_____(填序号)。

a.增大CO浓度
b.加压
c.恒容时充入氩气
d.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是

A.31d和33d属于同种核素
B.气态氢化物的稳定性:a>d>e
C.工业上常用电解法制备单质b
D.a和b形成的化合物不可能含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32.0 gCu投入50mL 12moL/L的浓硝酸中,充分反应后,收集到4.48L(标准状况)NO和NO2的混合气体。
(1)被还原硝酸的物质的量是_________mol。
(2)判断32.0gCu和50mL 12moL/L的硝酸反应后有剩余的是______________,剩余的物质物质的量为____________________,生成的NO气体体积为(标况下)_________________。
(3)如果往反应后的体系内再加入100mL2mol/L的稀硫酸,充分反应后又有气体逸出。写出反应的离子方程式并用单线桥法表示电子转移的方向和数目 _______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com