
【题目】常温下,将NaOH溶液分别加到HF溶液、CH3COOH溶液中,两混合溶液中离子浓度与pH的变化关系如图所示,已知pKa=-lgKa,下列有关叙述错误的是
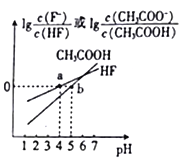
A. 常温下,Ka(CH3COOH)=10-5
B. a点时,c(F-)=c(HF)>c(Na+)>c(H+)>c(OH-)
C. 常温下,0.1mol/LNaF溶液的pH小于0.1mol/LCH3COONa溶液的pH
D. 向CH3COOH溶液中加入NaOH溶液后所得的混合溶液中, 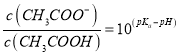
【答案】D
【解析】A、根据b点信息,可知pH=5时, 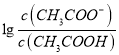 =0,即
=0,即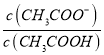 =1。所以Ka(CH3COOH)=
=1。所以Ka(CH3COOH)= 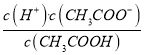 =c(H+)=10-5,故A正确。B、根据a点信息可知,pH=4,c(H+)>c(OH-),
=c(H+)=10-5,故A正确。B、根据a点信息可知,pH=4,c(H+)>c(OH-), 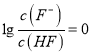 ,则c(F-)=c(HF);根据电荷守恒c(F-)+c(OH-)=c(H+)+c(Na+),则c(F-)>c(Na+),所以c(F-)=c(HF)>c(Na+)>c(H+)>c(OH-),故B正确。C、根据a点信息可知,Ka(HF)= c(H+)=10-4>Ka(CH3COOH);越弱越水解,所以同浓度的NaF溶液和CH3COONa溶液,后者水解程度较大,pH较大,故C正确。D、根据Ka(CH3COOH)=
,则c(F-)=c(HF);根据电荷守恒c(F-)+c(OH-)=c(H+)+c(Na+),则c(F-)>c(Na+),所以c(F-)=c(HF)>c(Na+)>c(H+)>c(OH-),故B正确。C、根据a点信息可知,Ka(HF)= c(H+)=10-4>Ka(CH3COOH);越弱越水解,所以同浓度的NaF溶液和CH3COONa溶液,后者水解程度较大,pH较大,故C正确。D、根据Ka(CH3COOH)= 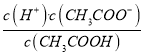 可知,
可知, 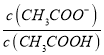 =
=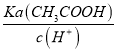 =
=![]() =10
=10![]() ,故D错误。故选D。
,故D错误。故选D。


科目:高中化学 来源: 题型:
【题目】A,B,C,D均为气体,在2A+B![]() 3C+5D反应中,表示该反应速率最快的是
3C+5D反应中,表示该反应速率最快的是
A. υ(A)= 0.5 mol/(L·s) B. υ(C)= 0.8 mol/(L·s)
C. υ(B)= 0.3 mol/(L·s) D. υ(D)= 1 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.淀粉、纤维素、油脂的相对分子质量都较大,所以都属于高分子化合物
B.苯、乙酸、乙醇在一定条件下都能发生取代反应,且都能与金属钠反应
C.乙烯能使酸性高锰酸钾和溴水褪色,二者反应原理相同
D.等物质的量的乙烷和乙醇完全燃烧时所需氧气的质量不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关离子浓度及pH大小的比较,正确的是( )
A. NH4+浓度相同的下列溶液:①(NH4)2Fe(SO4)2 ②(NH4)2CO3 ③(NH4)2SO4,溶液浓度由大到小的顺序是:③>②>①
B. 由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,其离子浓度不可能是:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C. pH=13的Ba(OH)2溶液与pH=1的HCl溶液等体积混合后,混合溶液的pH>7
D. pH=12的Ba(OH)2溶液与pH=14的NaOH溶液等体积混合,混合溶液的pH范围是13<pH<14
【答案】D
【解析】①(NH4)2Fe(SO4)2溶液中Fe2+的水解对于铵根离子的水解起到抑制作用, ②(NH4)2CO3 中碳酸根离子水解对于铵根离子的水解起到促进作用,③(NH4)2SO4溶液中硫酸根离子对铵根离子的水解无影响,所以溶液中铵根离子的水解程度的大小顺序为:②>③>①。则要达到相同的铵根离子浓度,水解程度大的溶液,物质的浓度应该越大,即溶液浓度由大到小的顺序是:②>③>①。选项A错误。由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,由于醋酸的浓度远大于氢氧化钠的浓度,所以中和以后得到醋酸钠(较少)和醋酸(较多)的混合溶液,溶液显酸性,即c(H+)>c(OH-),根据电荷守恒得到:c(CH3COO-)>c(Na+)。又因为钠离子是醋酸钠完全电离生成的,氢离子使醋酸微弱电离得到的,所以有c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。选项B错误。pH=13的Ba(OH)2溶液与pH=1的HCl溶液等体积混合,两溶液的氢氧根离子和氢离子的浓度刚好相等,等体积混合,恰好中和,溶液显中性。选项C错误。pH=12的Ba(OH)2溶液与pH=14的NaOH溶液等体积混合,其![]() ,所以
,所以![]() ,
, ![]() ,选项D正确。
,选项D正确。
【题型】单选题
【结束】
14
【题目】室温下,下列溶液中粒子浓度关系正确的是( )
A. Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4-)+c(H2C2O4)
B. 20mL0.1molL-1CH3COONa溶液与10mL0.1molL-1HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C. CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
D. pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根离子腐蚀,其电化学腐蚀原理如图所示。下列说法正确的是
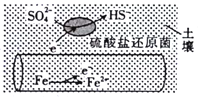
A. 铁管道发生的是吸氧腐蚀 B. 输送暖气的管道也易发生此类腐蚀
C. 这种情况下,土壤的pH增大 D. 管道上刷富铜油漆可以延缓管道的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿(主要成分是Cu2S)含铜量高,是最重要的炼铜矿石。
I.已知: ①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) △H=-768.2kJ.mol-1
②Cu2S(s)+O2(g)=2Cu(s)+SO2(g) △H=-217.4kJ.mol-1
(1)Cu2S与Cu2O反应生成Cu和SO2的热化学方程式为_____________。
Ⅱ.Cu2O可催化二甲醚合成乙醇。
反应①:CH3OCH3(g)+CO(g)![]() CH3COOCH3(g) △H1
CH3COOCH3(g) △H1
反应②:CH3COOCH3(g)+2H2(g)![]() CH3OH(g)+C2H5OH(g) △H2
CH3OH(g)+C2H5OH(g) △H2
(2)压强为pkPa时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图1所示,则△H1____(填“>”或“<”,下同)0、△H2_____0。温度对平衡体系中乙酸甲酯的含量和乙醇含量的影响如图2所示。在300~600K范围内,乙酸甲酯的百分含量逐渐增大,而乙醇的百分含量逐渐减小的原因是____________。

(3)若压强为pkPa、温度为800K时,向2L恒容密闭容器中充入1molCH3OCH3和1molCO发生反应①,2min时达到平衡,则前2min内CH3COOCH3的平均生成速率为_________,该条件下平衡常数K=_____________。
(4)以铜为原料,利用电解法可制取具有广泛用途的光电材料——纳米Cu2O,其工作原理如图3所示。则b是_______极,电解时阳极的电极反应式为______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中,不正确的是( )
A.氢氧化钡晶体与氯化铵晶体的反应属于放热反应
B.原电池工作时,通过外电路的电子和内电路的离子构成环路
C.元素的性质随着原子序数的递增而呈周期性变化的规律叫元素周期律
D.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com