
【题目】次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式:_______________________________________
(2)(H3PO2)中,磷元素的化合价为_________________
(3)H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:________填化学式)
(4)已知:甲醇脱水反应 ①2CH3OH(g)=CH3OCH3(g)+H2O(g) △H1=-23.9kJ·mol-1
甲醇制烯烃反应
②2CH3OH(g)=C2H4 (g)+2H2O(g) △H2=-29.1kJ·mol-1
乙醇异构化反应
③CH3CH2OH(g)=CH3OCH3(g)) △H3=+50.7kJ·mol-1
则乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g)的 △H=________kJ·mol-1
(5)下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系[(其中n(H2O)︰n(C2H4)=1︰1]
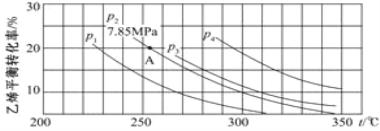
①列式计算乙烯水合制乙醇反应在图中A点的平衡常数K=________________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②图中压强P1、P2、P3、P4的大小顺序为:______,理由是:__________
【答案】 H3PO2 ![]() H++H2PO2- +1 H3PO4 -45.5 K=0.07(MPa)-1 P1< P2< P3< P4 反应分子数减少,相同温度下,压强升高,乙烯转化率提高
H++H2PO2- +1 H3PO4 -45.5 K=0.07(MPa)-1 P1< P2< P3< P4 反应分子数减少,相同温度下,压强升高,乙烯转化率提高
【解析】(1)H3PO2是一元中强酸,溶液中部分电离出氢离子,所以其电离方程式为H3PO2![]() H2PO2-+H+;(2)H3PO2中,总化合价为0,其中氢元素为+1价,氧元素为-2价,则P元素的化合价为+1价;(3)该反应中Ag+为氧化剂,H3PO2为还原剂,氧化剂与还原剂的物质的量之比为4:1。设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1-0)=1×(x-1),解得x=5,所以氧化产物为+5价的H3PO4;(4)已知:
H2PO2-+H+;(2)H3PO2中,总化合价为0,其中氢元素为+1价,氧元素为-2价,则P元素的化合价为+1价;(3)该反应中Ag+为氧化剂,H3PO2为还原剂,氧化剂与还原剂的物质的量之比为4:1。设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1-0)=1×(x-1),解得x=5,所以氧化产物为+5价的H3PO4;(4)已知:
①2CH3OH(g)=CH3OCH3(g)+H2O(g) △H1=-23.9kJ·mol-1
②2CH3OH(g)=C2H4 (g)+2H2O(g) △H2=-29.1kJ·mol-1
③CH3CH2OH(g)=CH3OCH3(g)) △H3=+50.7kJ·mol-1
根据盖斯定律可知①-②-③即得到乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g) 的反应热△H=-45.5 kJ·mol-1。
(5)①该温度下,乙烯的转化率为0.2,设起始时乙烯和水的物质的量为nmol,则反应的乙烯和水的物质的量分别为0.2nmol,平衡时两者的物质的量均为0.8nmol;生成的乙醇的物质的量为0.2nmol,平衡时总的物质的量为1.8nmol,乙烯、水、乙醇的物质的量分数分别为0.8/1.8,0.8/1.8,0.2/1.8,因此乙烯水合制乙醇反应在图中A点的平衡常数为 (MPa)-1;②由方程式C2H4 (g) + H2O(g)=C2H5OH(g)可知该反应的正反应是气体体积减小的反应,所以增大压强,平衡正向移动,乙烯的转化率提高,因此压强关系是:P1< P2< P3< P4。
(MPa)-1;②由方程式C2H4 (g) + H2O(g)=C2H5OH(g)可知该反应的正反应是气体体积减小的反应,所以增大压强,平衡正向移动,乙烯的转化率提高,因此压强关系是:P1< P2< P3< P4。


科目:高中化学 来源: 题型:
【题目】下列各组物质中,均属于共价化合物并且化学键类型完全相同的是( )
A. N2和H2 B. H2S和CO2 C. O2和CCl4 D. Cl2和NH4NO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用N2与Mg制备Mg3N2的装置如图所示(焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是( )

A. ①、②、③中依次盛装浓H2SO4溶液、NaOH溶液、焦性没食子酸溶液
B. 实验操作顺序为:通空气→管式电炉⑤通电加热→管式电炉④通电加热
C. ④的作用是预热经净化后的氮气
D. 当⑤的瓷舟中燃烧产生白光时,⑤可停止通电加热装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在生产、生活中有着重要的作用。

请回答下列问题:
(1)图1是常温下1 mol NO2和1 mol CO反应生成CO2和NO过程中的能量变化示意图,请写出NO2和CO反应的热化学方程式:____________________________。
(2)如图2,在恒温、恒容的密闭容器中,通入一定量的N2O4发生反应N2O4(g)![]() 2NO2(g) ΔH。
2NO2(g) ΔH。
①在0~60 s时间段,反应速率v(N2O4)为____ mol·L-1·s-1。
②温度升高,混合气体的颜色变深,则ΔH____0(填“>”或“<”)。
③改变条件重新达到平衡时,要使N2O4的体积分数变大,可采取的措施有____(填字母)。
a.向混合气体中通入N2O4 b.升高温度
c.向混合气体中通入NO2 d.使用高效催化剂
(3)实验室可用NaOH溶液吸收NO2,发生反应的化学方程式为2NO2+2NaOH![]() NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1 L溶液A,溶液B为0.1 mol·L-1的CH3COONa溶液。
NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1 L溶液A,溶液B为0.1 mol·L-1的CH3COONa溶液。
①A、B两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为_________________。
(HNO2的电离常数Ka=7.1×10-4 mol·L-1,CH3COOH的电离常数Ka=1.7×10-5 mol·L-1)。
②可使A、B两溶液的pH相等的方法是____(填字母)。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(4)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将化学方程式表示为Cu+HNO3![]() Cu(NO3)2+NO↑+NO2↑+H2O(方程式未配平)。0.6 mol Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量为____。
Cu(NO3)2+NO↑+NO2↑+H2O(方程式未配平)。0.6 mol Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于化学反应:N2(g)+O2(g) ![]() 2NO(g),在密闭容器中,判断下列条件的改变引起该反应的正反应速率的变化(用“增大”“不变”“减小”表示)及平衡的移动(用“正向”“逆向”或“不”表示)。
2NO(g),在密闭容器中,判断下列条件的改变引起该反应的正反应速率的变化(用“增大”“不变”“减小”表示)及平衡的移动(用“正向”“逆向”或“不”表示)。
A.体积不变充入N2使压强增大ν正__________,平衡__________移动。
B.压强不变充入氩气使体积增大ν正__________________,平衡__________移动。
C.增大体积使压强减小ν正__________________,平衡__________移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象和用途中,浓硫酸表现脱水性的是( )
A. 实验室制取氯气时浓硫酸作干燥剂 B. 浓硫酸使火柴梗变黑
C. 浓硫酸加到胆矾上,蓝色晶体变成白色粉末 D. 浓硫酸使Fe、Al钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素及其化合物的性质是化学研究的主要内容之一。下列叙述正确的是
A. 向Fe(NO3)2溶液中滴加稀盐酸,溶液变黄
B. Na与氧气反应只生成Na2O2
C. 将SO2通入过量BaCl2溶液可生成BaSO3沉淀
D. 向酚酞试液中加足量Na2O2粉末,充分振荡后溶液呈红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com