
| T/℃ | 25 | 80 | 230 |
| K | 5×104 | 1 | 2×10-5 |
分析 图表的反应平衡常数随温度升高减小,说明升温平衡逆向进行,正反应为放热反应,
(1)反应是放热反应,升温平衡逆向进行,Ni的转化率减小;
(2)要提高上述反应中Ni的转化率,应使平衡正向进行,结合影响化学平衡的因素分析判断.
解答 解:图表的反应平衡常数随温度升高减小,说明升温平衡逆向进行,正反应为放热反应,
(1)Ni(s)+4CO(g)$\stackrel{50℃}{?}$Ni(CO)4(g).反应是放热反应,升温平衡逆向进行,Ni的转化率减小,故答案为:减小;
(2)要提高上述反应中Ni的转化率,应使平衡正向进行,反应是气体体积减小的放热反应,可以增大压强、降低温度、增加一氧化碳的浓度等措施,
故答案为:增大压强或降低温度或增加一氧化碳的浓度.
点评 本题考查了影响化学平衡的因素分析,平衡常数随温度变化判断反应能量变化,平衡移动原理和反应特征分析是解题关键,题目较简单.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:选择题
| A. | 一分子O4由两分子O2构成 | |
| B. | O4是一种单质 | |
| C. | 等质量的O4和O2含有相同数目的分子 | |
| D. | O4是一种化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; 的系统命名为3-甲基戊烷;
的系统命名为3-甲基戊烷;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室制备1,2-二溴乙烷的反应原理如下:C2H5OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br,可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:
实验室制备1,2-二溴乙烷的反应原理如下:C2H5OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br,可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:| 本题中出现有机物相关数据 | |||
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
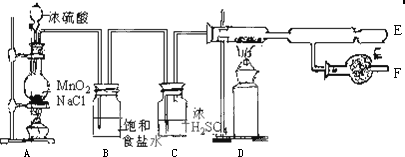
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(B)=0.25 mol•L-1•s-1 | B. | C的体积分数为30% | ||
| C. | B的转化率为25% | D. | n=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉与氯化铁溶液混合:Fe+Fe3+=2Fe2+ | |
| B. | 氯化铝溶液与氨水反应:Al3++3OH-=Al(OH)3↓ | |
| C. | 碳酸钙与稀盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| D. | 醋酸与氢氧化钠溶液反应:CH3COOH+OH-=CH3COO-+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com