
| A£® | ÓĆ²£Į§°ōÕŗČ”CH3COOHČÜŅŗ£¬µćŌŚÓĆĖ®ŹŖČóµÄpHŹŌÖ½ÉĻ²ā¶ØĘäpH | |
| B£® | ÓĆ25ml¼īŹ½µĪ¶Ø¹ÜĮæČ”20.00 mL KMnO4ČÜŅŗ | |
| C£® | ĪŖ³żČ„±½ÖŠµÄÉŁĮæ±½·Ó£¬Ļņ»ģŗĻĪļÖŠ¼ÓČėŹŹĮæµÄĒāŃõ»ÆÄĘŗó·ÖŅŗ | |
| D£® | 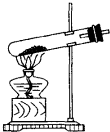 ÓĆČēĶ¼×°ÖĆ¼ÓČČ·Ö½āNaHCO3 |
·ÖĪö A£®pHŹŌÖ½²»ÄÜŹĀĻČŹŖČó£»
B£®øßĆĢĖį¼Ų¾ßÓŠŃõ»ÆŠŌ£¬øÆŹ“ĻšĘ¤¹Ü£»
C£®±½Óė±½·Ó»„ČÜ£¬µ«±½·ÓÓėNaOHČÜŅŗ·“Ó¦ŗó£¬Óė±½·Ö²ć£»
D£®ŹŌ¹ÜæŚÓ¦ĀŌĻņĻĀĒ抱£®
½ā“š ½ā£ŗA£®²ā¶Ø“×ĖįpH£¬pHŹŌÖ½²»ÄÜŹĀĻČŹŖČ󣬷ĄÖ¹“×Ėį±»Ļ”ŹĶ¶ųµ¼ÖĀ²ā¶Ø½į¹ūĘ«“󣬹ŹA“ķĪó£»
B£®øßĆĢĖį¼Ų¾ßÓŠŃõ»ÆŠŌ£¬øÆŹ“ĻšĘ¤¹Ü£¬Ó¦ÓĆĖįŹ½µĪ¶Ø¹Ü£¬¹ŹB“ķĪó£»
C£®¼ÓČėĒāŃõ»ÆÄĘČÜŅŗŗ󣬱½·ÓÓėNaOH·“Ó¦£¬³ä·ÖÕńµ“£¬¾²ÖĆŗóÓė±½·Ö²ć£¬ŌņŃ”Ōń·ÖŅŗ·Ø³żŌÓ£¬¹ŹCÕżČ·£»
D£®ŹŌ¹ÜæŚÓ¦ĀŌĻņĻĀĒ抱£¬·ĄÖ¹Ė®ÕōĘųĄäÄż»ŲĮ÷£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°»ł“”ŹµŃé²Ł×÷£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŹµŃéÄÜĮ¦µÄ漲飬ĪŖøßĘµæ¼µć£¬×¢Ņā°ŃĪÕŹµŃéµÄ·½·Ø”¢²½ÖčŗĶŹ¹ÓƵÄŅĒĘ÷£¬×¢ÖŲĻą¹Ų»ł“”ÖŖŹ¶µÄ»żĄŪ£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | A·Ö×ÓµÄŌ×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ŹĒ1s22s22p63s23p4 | |
| B£® | ĻņDµÄČÜŅŗÖŠ¼ÓČėÉŁĮ涞Ńõ»ÆĆĢ£¬Ņ»¶ØÓŠĪŽÉ«ĘųĢåÉś³É£® | |
| C£® | »¹ŌŠŌĒæČõB£¾C | |
| D£® | Čō½«1mol EŌŚŃõĘųÖŠĶźČ«Č¼ÉÕ£¬Ö»Éś³É1mol CO2ŗĶ2molH2O£¬ŌņEµÄ·Ö×ÓŹ½ŹĒCH4O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 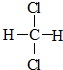 ŗĶ ŗĶ  | B£® | CH2=CH-CH=CH2ŗĶ  | ||
| C£® | 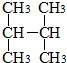 ŗĶ ŗĶ 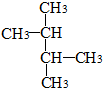 | D£® | C£ØCH3£©3C£ØCH3£©3ŗĶCH3£ØCH2£©3C£ØCH3£©3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1molAlCl3ŌŚČŪȌדĢ¬Ź±Ąė×Ó×ÜŹżĪŖ0.4NA | |
| B£® | 2.2 g·Ö×ÓŹ½ĪŖ 2H218OµÄĖ®ÖŠŗ¬ÓŠµÄÖŠ×ÓŹżĪŖ1.2 NA | |
| C£® | µē½ā±„ŗĶŹ³ŃĪĖ®Ź±£¬µ±Ņõ¼«²śÉśH2 22.4LŹ±£¬µēĀ·ÖŠ×ŖŅʵĵē×ÓŹżĪŖ2NA | |
| D£® | ³£ĪĀĻĀpH=1µÄH2SO4ČÜŅŗÖŠ£¬H+µÄÅضČĪŖ0.2mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬Cl2µÄĦ¶ūÖŹĮæĪŖ71g | |
| B£® | Ńõ»Æ»¹Ō·“Ó¦Ņ»¶ØÓŠŃõŌŖĖŲ²Ī¼Ó | |
| C£® | ±ź×¼×“æöĻĀ£¬1 mol CCl4µÄĢå»żŹĒ22.4L | |
| D£® | Na2CO3ŹōÓŚÄĘŃĪ£¬ÓÖŹōÓŚĢ¼ĖįŃĪŹĒÓĆ½»²ę·ÖĄą·Ø·ÖĄąµÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗĻ½šµÄµ¼µēŠŌ±Č³É·Ö½šŹōĒæ | |
| B£® | ŗĻ½šµÄæ¹øÆŹ“ŠŌÄܶ¼ŗÜŗĆ | |
| C£® | ŗĻ½šµÄ»śŠµĒæ¶Č±Čø÷³É·Ö½šŹōŠ” | |
| D£® | ¶ąŹżŗĻ½š±Č³É·Ö½šŹōČŪµćµĶ£¬Ó²¶Č“ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com