
���� ��1�����ݸ�����ķ���ʽ��ɼ��������֮�ȣ����ʵ���������������ȣ�����m=nM������������֮�ȣ�
��2������n=$\frac{m}{M}$���㰱�����ʵ������ٸ���V=nVm���㰱����������Hԭ����Ŀ��ȼ����������ʵ������ٸ���V=nVm��������������
��3�������6.72LSO2�����ʵ���Ϊ��$\frac{6.72L}{22.4L/mol}$=0.3mol��1L0.6mol•L-1NaOH��Һ��NaOHΪ1L��0.6mol/L=0.6mol���������ʵ���֮��Ϊ0.3mol��0.6mol=1��2��������Ӧ��SO2+2NaOH=Na2SO3+H2O����֪n��Na2SO3��=n��SO2�����ٸ���c=$\frac{n}{V}$����c��Na2SO3����
��� �⣺��1����ԭ������ͬ����������SO2��CO��NO��������֮��=$\frac{1}{2}$��1��1=1��2��2��SO2��CO��NO�����ʵ���֮�ȵ����������֮�ȣ���SO2��CO��NO������֮��=��64g/mol��1������28g/mol��2������30g/mol��2��=16��14��15��
�ʴ�Ϊ��1��2��2��16��14��15��
��2����״���£�4.25g NH3�����ʵ���Ϊ��$\frac{4.25g}{17g/mol}$=0.25mol�������Ϊ0.25mol��22.4L/mol=5.6L����֮������ͬ��Ŀ����ԭ�ӵ�����Ϊ��$\frac{0.25mol��3}{2}$=0.375mol����������������Ϊ��0.25mol��22.4L/mol=8.4L��
�ʴ�Ϊ��5.6��8.4��
��3�������6.72LSO2�����ʵ���Ϊ��$\frac{6.72L}{22.4L/mol}$=0.3mol��1L0.6mol•L-1NaOH��Һ��NaOHΪ1L��0.6mol/L=0.6mol���������ʵ���֮��Ϊ0.3mol��0.6mol=1��2��������Ӧ��SO2+2NaOH=Na2SO3+H2O�����õ���������Na2SO3����֪n��Na2SO3��=n��SO2��=0.3mol����c��Na2SO3��=$\frac{0.3mol}{1L}$=0.3mol/L��
�ʴ�Ϊ��Na2SO3��0.3��
���� ���⿼�������ʵ����ļ��㣬��Ŀ�Ѷ��еȣ���ȷ���ʵ�����Ħ������������Ħ�����������٤�����������ʵ���Ũ�ȵ�֮��Ĺ�ϵΪ���ؼ�������������ѧ���Ļ�ѧ����������


 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3 | B�� | 4 | C�� | 5 | D�� | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ���� |
| A | ��18O���Ҵ������ᷴӦ�Ʊ�����������Ӧ��18O�������κ������� | �ԣ���Ϊ�˷�ӦΪ���淴Ӧ |
| B | ����������Һ��ͨ��CO2�����Ʊ��õ����ӣ����õ�̼������ | �ԣ�����ǿ��������Ĺ��ɣ�̼������Աȱ��ӵ�����ǿ���ʿ��ô˷�Ӧ�Ʊ����� |
| C | ��±����ˮ������Һ��ֱ�Ӽ���AgNO3��Һ�����ݳ�����ɫ�����ж�±��ԭ������ | �ԣ�ˮ�����Һ����±���⣬��AgNO3��Һ��Ӧ����±�������� |
| D | �����Ը��������Һ��ȥ�����е���ϩ���� | �ԣ���ϩ�������Ը��������Һ��Ӧ�������鲻������������Һ��Ӧ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$3SO2��+2H2O | |
| B�� | NaCl��s��+H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$NaHSO4+HCl�� | |
| C�� | 2FeO+4H2SO4��Ũ���TFe2��SO4��3+SO2��+4H2O | |
| D�� | C+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+2SO2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ����������������Һ��Ӧ��H++OH-�TH2O | |
| B�� | ����������ˮ��Ӧ��2Na2O 2+2H2O�T4Na++4OH-+O2�� | |
| C�� | �������������Fe2O3+6H+�T2Fe3++3H2O | |
| D�� | Na������ͭ��Һ��Ӧ��2Na+Cu2+�T2Na++Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
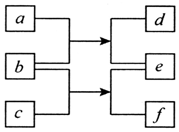 ������Ԫ��W��X��Y��Z��ԭ�������������ӣ�������Ԫ����ɵĸ�����ת����ϵ��ͼ��ʾ������bΪ���ʣ���ˮ��Һ�������Ҿ���Ư���ԣ�dΪ�����Ҿ���ͬ�������壻������0.0l mol•L-1f��Һ��pH��2������˵����ȷ���ǣ�������
������Ԫ��W��X��Y��Z��ԭ�������������ӣ�������Ԫ����ɵĸ�����ת����ϵ��ͼ��ʾ������bΪ���ʣ���ˮ��Һ�������Ҿ���Ư���ԣ�dΪ�����Ҿ���ͬ�������壻������0.0l mol•L-1f��Һ��pH��2������˵����ȷ���ǣ�������| A�� | ԭ�Ӱ뾶�Ĵ�СW��Y��Z | B�� | Ԫ�صķǽ�����Z��X��Y | ||
| C�� | Y��������һ��Ϊ���������� | D�� | Z�ĺ�����һ��Ϊǿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe+2HCl�TFeCl2+H2 | B�� | CH4$\frac{\underline{\;����\;}}{\;}$C+2H2 | ||
| C�� | Mg��OH��2+2HCl�TMgCl2+2H2O | D�� | CaCO3$\frac{\underline{\;����\;}}{\;}$CaO+CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������HCl��Cl2ͨ�뱥��NaHCO3��Һ�г�ȥHCl | |
| B�� | �ó���ʯ��ˮ����NaHCO3��Na2CO3 | |
| C�� | ��BaCl2��Һ����SO42-��SO32- | |
| D�� | ��ŨHNO3��Cu��Ӧ�Ʊ�NO2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com