
| A. | C (s)+O2(g)=CO (g)△H=-110.5 kJ/mol | |
| B. | C (s)+O 2(g)=CO2(g)△H=-393.5 kJ/mol | |
| C. | 2H2(g)+O2(g)=2H2O (l)△H=-571.6 kJ/mol | |
| D. | H2(g)+$\frac{1}{2}$O2(g)=H2O (g)△H=-241.8 kJ/mol |
分析 燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,
A.碳的燃烧为放热反应,焓变应该小于0;
B.根据燃烧热的概念及热化学方程式的书写原则分析;
C.氢气燃烧热的热化学方程式中,氢气的计量数必须为1;
D.氢气的燃烧热中,生成水的状态必须液态.
解答 解:A.C燃烧生成的稳定氧化物是CO2不是CO,且焓变为负值,所以不符合燃烧热的概念要求,故A错误;
B.1molC完全燃烧生成稳定的CO2,符合燃烧热的概念要求,该反应放出的热量为燃烧热,故B正确;
C.燃烧热是指1mol纯净物完全燃烧,方程式中氢气的系数为2mol,不是氢气的燃烧热,故C错误;
D.燃烧热的热化学方程式中生成的氧化物必须为稳定氧化物,水为液态时较稳定,故D错误;
故选B.
点评 本题考查热化学方程式的书写方法,题目难度不大,明确燃烧热达到概念为解答关键,注意掌握热化学方程式的书写原则,试题培养了学生的灵活应用能力.


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:选择题

| A. | 1 mol莽草酸完全燃烧消耗156.8 L O2 | |
| B. | 1 mol莽草酸最多与4 mol Na发生反应 | |
| C. | 莽草酸能使溴的四氯化碳溶液褪色 | |
| D. | 莽草酸可发生聚合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:K+、NO3-、SO32-、Na+ | |
| B. | 使石蕊呈红色的溶液中:Na+、HCO3-、NO3-、AlO2- | |
| C. | 使pH试纸显红色的溶液中:Cu2+、Fe3+、NO3-、SO42- | |
| D. | 在酸性溶液中:NH4+、Na+、Cu2+、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第一步 | B. | 第二步 | C. | 第三步 | D. | 第四步 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
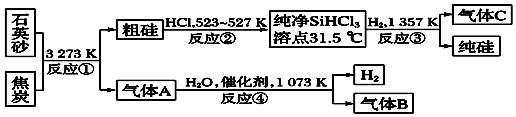
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 950 mL | B. | 500 mL | C. | 1 000 mL | D. | 任意规格 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
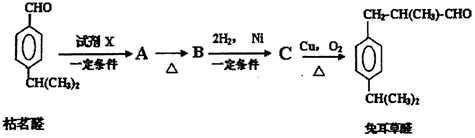
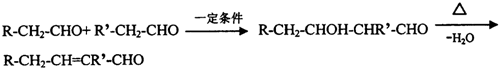
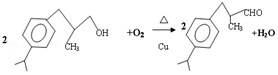 .
.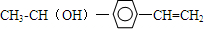 、
、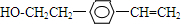 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
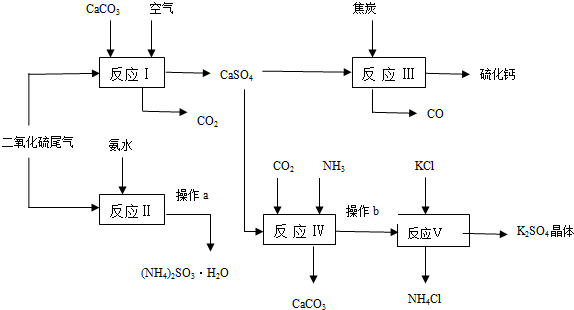
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com