
下列事实中,不能用勒沙特列原理解释的是
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫
B.在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化
C.温度过高对合成氨不利
D.常温下,将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015湖北省荆门市高一上学期期末考试化学试卷(解析版) 题型:计算题
把5.1g镁铝合金的粉末放入500mL1mol·L-1盐酸中,恰好完全反应。试计算:
(1)该合金中镁和铝的物质的量。
(2)将等质量的该合金投入到足量的氢氧化钠溶液中,求标况下放出气体的体积。
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邯郸市高一上学期期末考试化学试卷(解析版) 题型:选择题
在无色透明溶液中可以大量共存的离子组是
A.H+、Na+、Cl-、AlO2-
B.Al3+、NO3-、SO42-、MnO4-
C.K+、Ca2+、OH-、HCO3-
D.NH4+、NO3-、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邯郸市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列事实能说明甲酸(HCOOH)属于弱酸的是
①1mol·L-1 HCOOH溶液的pH=2 ②甲酸能与水以任意比互溶
③20mL 1mol·L-1HCOOH与20mL 1mol·L-1NaOH恰好中和 ④HCOONa溶液的pH>7
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邯郸市高二上学期期末考试化学试卷(解析版) 题型:选择题
已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16 ,Ksp(AgBr)=7.7×10-13,则下列难溶盐的
饱和溶液中,Ag+浓度大小顺序正确的是
A.AgCl>AgI> AgBr B.AgCl> AgBr>AgI
C.AgBr >AgCl>AgI D.AgBr >AgI>AgCl
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高一上学期期末考试化学试卷(解析版) 题型:实验题
(10分)某化学兴趣小组进行铁跟水蒸气反应的实验,实验装置如下,发现有黑色晶体生成并产生无色气体,他们继续对反应产物进行探究。
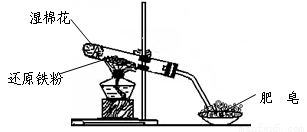
已知:①FeO + 2H+ = Fe2+ + H2O
②Fe2O3 + 6H+ = 2Fe3+ +3 H2O
③Fe3O4 + 8H+ = Fe2+ +2Fe3+ +4 H2O
请回答下列问题:
(1)该组同学欲确定反应一段时间后试管中固体的成分,设计如下实验方案:
①待试管冷却后,取少许其中的固体溶于稀硫酸得溶液B。
②取少量溶液B滴加KSCN溶液,若溶液变红色,则说明试管中固体物质的成分是(只有一个选项符合题意) ,若溶液未变红色,则说明试管中固体物质的成分是(只有一个选项符合题意) 。
A.一定有Fe3O4,可能有Fe
B.只有Fe(OH)3
C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe
E.只有Fe3O4
(2)该组同学取少量溶液B进行了实验,结果②中溶液未变红色,原因是(用离子方程式表示) 。
(3)铁跟水蒸气反应的化学方程为 。
(4)该组同学另取少量溶液B,使其跟NaOH溶液反应。若按下图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出沉淀由白色变成灰绿色最后变成红褐色的反应方程式 。
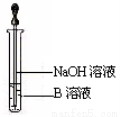
(5)一段时间后,该组同学发现(2)中未变红色的溶液变成红色,说明Fe2+具有 (填化学性质)。由此可知,实验室中含Fe2+的盐溶液需现用现配,并且配制含Fe2+的盐溶液时应加入少量 。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.氢氧化钠与氯化铜溶液:2OH-+Cu2+===Cu(OH)2↓
B.石灰石与盐酸:CO32-+2H+===CO2↑+H2O
C.氯气与碘化钾溶液:Cl2+2 I- = 2 I + 2 Cl-
D.用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-===2AlO2-+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高二第一学期期末化学试卷(解析版) 题型:填空题
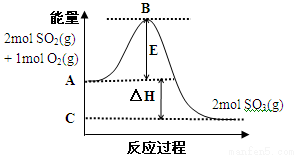
(7分)2SO2(g) + O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99 kJ·mol-1。
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99 kJ·mol-1。
请回答下列问题:
 (1)已知图中C 点表示2mol SO3(g)的总能量,则A点表示: ;E所代表的能量是 ;E的大小对该反应的反应热 影响。(填“有”或“无”)。
(1)已知图中C 点表示2mol SO3(g)的总能量,则A点表示: ;E所代表的能量是 ;E的大小对该反应的反应热 影响。(填“有”或“无”)。
 (2)图中△H= kJ·mol-1。
(2)图中△H= kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省龙岩市非一级达标校高一上学期期末化学试卷(解析版) 题型:填空题
(10分)某无色透明溶液中只可能大量存在OH-、Cl-、Na+、Mg2+、Cu2+中的几种离子。
(1)溶液显无色,说明原溶液中不存在的离子是_______;
(2)取少量原溶液加入铝粉有气体放出,说明原溶液中肯定存在的离子是___________;该反应除产生气体外,另一种生成物的化学式是_________________;
(3)另取少量原溶液加入过量稀硝酸,再加几滴AgNO3溶液,出现白色沉淀。
该过程中发生2个反应,对应的离子方程式是 、 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com