
| V |
| 2 |
A、
| ||
B、
| ||
C、
| ||
| D、125a/54Vmol/L |
| m |
| M |
| n |
| V |
| ag |
| 27g/mol |
| a |
| 27 |
| a |
| 27 |
| 0.5VmL |
| VmL |
| a |
| 54 |
| a |
| 54 |
| 3 |
| 2 |
| a |
| 36 |
| ||
| 4V×10-3L |
| 125a |
| 18V |


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
| A、反应后所得溶液呈酸性 |
| B、混合前两溶液的物质的量浓度相等 |
| C、原氨水中约有1%的含氮粒子为NH4+ |
| D、所得溶液中NH4+、NH3?H2O与NH3三种粒子的浓度之和为0.1 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴入酚酞的NaOH溶液中通入SO2气体红色消失 |
| B、溴水中通入SO2气体后溶液褪色 |
| C、酸性KMnO4溶液中通入SO2气体后溶液褪色 |
| D、品红溶液中通入SO2气体红色消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
| B、0.1 mol/L AgNO3溶液:H+、K+、SO42-、I- | ||
| C、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- | ||
| D、甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3 NaHCO3 NaCl NH4Cl |
| B、NaHCO3 Na2CO3 NH4Cl NaCl |
| C、(NH4)2SO4 NH4Cl NaNO3 Na2S |
| D、NH4Cl (NH4)2SO4 Na2S NaNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
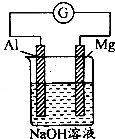 将Mg条、Al条平行插入一定浓度的NaOH溶液中(如图所示连接).此电池工作时,下列叙述正确的是( )
将Mg条、Al条平行插入一定浓度的NaOH溶液中(如图所示连接).此电池工作时,下列叙述正确的是( )| A、Mg比Al活泼,失去电子被氧化成Mg2+ |
| B、Al条在反应中逐渐变细 |
| C、该电池的外电路中,电子由Mg极流出,Al极流入 |
| D、消耗24gMg,电路中将转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放热反应的反应速率总是大于吸热反应的反应速率 |
| B、已知一定条件下石墨转化为金刚石吸收热量,则石墨比金刚石稳定 |
| C、对于吸热反应,生成物总能量一定低于反应物总能量 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④⑥⑦ | B、①②⑤ |
| C、②⑦⑧ | D、①⑤⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com