
【题目】下列有关说法正确的是( )
A. 2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0
B. 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
C. CH3COOH 溶液加水稀释后,溶液中![]() 的值增大
的值增大
D. Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解向左移动,溶液的pH 增大
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 1mol O的质量是16 g/mol B. Na+的摩尔质量是23 g
C. CO2的摩尔质量是44 g/mol D. 氢的摩尔质量是2 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在500 ℃时,2SO2(g)+O2(g) ![]() 2SO3(g)正向是放热反应的体系中,只改变下列条件,请把影响结果填入表中。
2SO3(g)正向是放热反应的体系中,只改变下列条件,请把影响结果填入表中。
改变条件 | 正反应速率 | 逆反应速率 | 平衡移动情况 |
(1)增大O2的浓度 | |||
(2)增大SO2的浓度 | |||
(3)减小SO3的浓度 | |||
(4)增大压强 | |||
(5)升高温度 | |||
(6)加入催化剂 | |||
(7)体积不变充入氖气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究某矿石(仅含两种元素)的组成和性质,设计并完成如下实验:
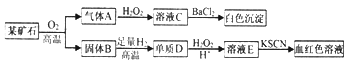
请回答:(1)某矿石的组成元素为__________(用元素符号表示)。
(2)气体A与H2O2溶液反应的化学方程式是________________。
(3)写出D→E的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1molH2(g)与1molBr2(g)完全反应生成2molHBr(g)放出102kJ的能量,方程式为:H2(g)+Br2(g)=2HBr(g);又知:
H2(g) | Br2(g) | HBr(g) | |
1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | a | 369 |
则表中a为
A. 200 B. 260 C. 404 D. 230
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活息息相关,下列叙述错误的是
A.用聚乙烯塑料代替聚乳酸塑料可减少白色污染
B.乙烯可作水果的催熟剂
C.大量燃烧化石燃料是造成雾霾天气的一种重要因素
D.含重金属离子的电镀废液不能随意排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
B. 向Cr2O72- + H2O![]() 2CrO42-+ 2H+ 的平衡体系中滴加10~20滴6mol/LNaOH溶液颜色由橙色变黄色
2CrO42-+ 2H+ 的平衡体系中滴加10~20滴6mol/LNaOH溶液颜色由橙色变黄色
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为 N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
D. 已知:
共价键 | C-C | C=C | C-H | H-H |
键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
则可以计算出反应 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项中所列举的物质与所属类别对应不正确的是
A.酸性氧化物:CO2、SO2、SiO2、Cl2O7
B.非电解质:蔗糖、四氯化碳、氨气、氯气
C.同素异形体:石墨与金刚石、单斜硫与斜方硫
D.混合物:铝热剂、纯净矿泉水、水玻璃、焦炉气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.氮的氧化物和碳的氧化物的排放是酸雨形成的主要原因
B.汽车尾气中的NO主要是由空气中的氮气在内燃机的高温下参与反应生成的
C.硫的氧化物的排放是光化学烟雾形成的主要原因
D.ClO2因为具有强还原性可用于杀菌消毒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com