
| A. | 漂白粉或漂粉精长期暴露在空气中会变质:Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO 2HClO=2 HCl+O2↑ | |
| B. | FeCl3溶液中加入铁粉,震荡后滴入几滴KSCN溶液,未见溶液变红:2Fe3++Fe═3 Fe2+ | |
| C. | 把水加入盛有过氧化钠固体的试管中,放出气体,可使带火星的木条复燃:2Na2O2+2 H2O═4 NaOH+O2↑ | |
| D. | 溶质物质的量之比为1:2的明矾溶液与 Ba(OH)2溶液混合,生成白色沉淀:Al3++2SO42-+2Ba2++4 OH-═2 BaSO4↓+Al(OH)3↓+H2O |
分析 A.次氯酸钙与二氧化碳、水反应生成的次氯酸易分解,导致漂白粉或漂粉精变质;
B.铁离子与铁粉反应生成亚铁离子,亚铁离子不会与硫氰化钾溶液反应;
C.过氧化钠与水反应生成氧气,可使带火星的木条复燃;
D.明矾与氢氧化钡按照物质的量1:2反应时,铝离子与氢氧根离子的物质的量之比为1:4,二者恰好反应生成偏铝酸根离子,不会生成氢氧化铝沉淀.
解答 解:A.漂白粉或漂粉精长期暴露在空气中发生反应:Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO、2HClO=2HCl+O2↑,导致变质,故A正确;
B.FeCl3溶液中加入铁粉,由于发生反应:2Fe3++Fe═3Fe2+,铁离子消失,震荡后滴入几滴KSCN溶液,溶液不会变红,故B正确;
C.把水加入盛有过氧化钠固体的试管中发生反应:2Na2O2+2 H2O═4 NaOH+O2↑,放出的氧气可使带火星的木条复燃,故C正确;
D.溶质物质的量之比为1:2的明矾溶液与 Ba(OH)2溶液混合,铝离子完全转化成偏铝酸根离子,正确的离子方程式为:Al3++SO42-+Ba2++4OH-═2BaSO4↓+AlO2-+2H2O,故D错误;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度中等,注意明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:实验题
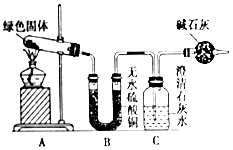 铜器久置,表面会生成一层绿色固体,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,得知该绿色物质是碱式碳酸铜.该小组同学利用如图装置进行实验,探究碱式碳酸铜的分解产物.
铜器久置,表面会生成一层绿色固体,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,得知该绿色物质是碱式碳酸铜.该小组同学利用如图装置进行实验,探究碱式碳酸铜的分解产物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
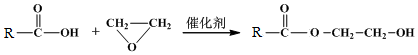
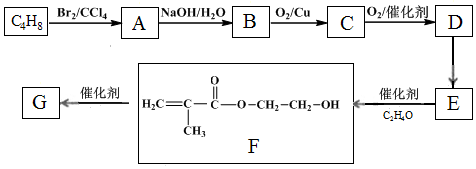
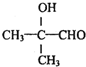 .
.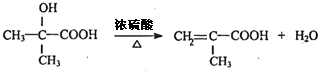 .
.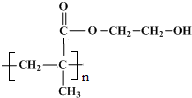 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| B. | NaHCO3溶液中加入盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | FeSO4溶液与稀硝酸反应:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O | |
| D. | “84消毒液”和“洁厕灵”(主要成分为盐酸)混合使用会产生有毒气体:ClO3-+5Cl-+6H+═3Cl2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15种 | B. | 16种 | C. | 17种 | D. | 18种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
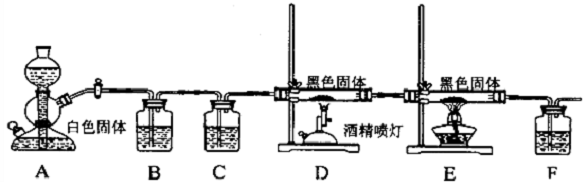
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com