
| A. | 标准状况下,22.4LH2O含有的分子数为NA | |
| B. | 在常温和常压下,22gCO2含有的分子数为0.5NA | |
| C. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA | |
| D. | 在同温、同压下,相同体积的任何气体,所含分子数相同 |
分析 A、标况下水为液体;
B、求出二氧化碳的物质的量,然后根据分子个数N=nNA来分析;
C、溶液体积不明确;
D、同温同压下相同体积的任何气体的物质的量相同.
解答 解:A、标况下水为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、22g二氧化碳的物质的量为0.5mol,而分子个数N=nNA=0.5NA个,故B正确;
C、溶液体积不明确,故溶液中的氯离子的个数无法计算,故C错误;
D、同温同压下相同体积的任何气体的物质的量相同,而分子个数和物质的量成正比,故当物质的量相同时,分子个数相同,故D正确.
故选BD.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
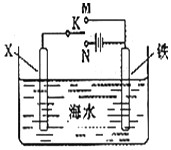 利用如图装置,可以模拟铁的电化学防护. 若X为碳棒,为减缓铁的腐蚀,开关K应该置于N(填M或者N)处,此时溶液中的阴离子向X极(填X或铁)移动.若X为锌,开光K置于M处,该电化学防护法称为:牺牲阳极的阴极保护法.
利用如图装置,可以模拟铁的电化学防护. 若X为碳棒,为减缓铁的腐蚀,开关K应该置于N(填M或者N)处,此时溶液中的阴离子向X极(填X或铁)移动.若X为锌,开光K置于M处,该电化学防护法称为:牺牲阳极的阴极保护法.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L的KNO3 溶液500 ml | B. | 0.05mol/L的K2SO4 溶液300ml | ||
| C. | 0.04mol/L的K3PO4 溶液100 ml | D. | 0.06mol/L的KHCO3 溶液120 ml |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
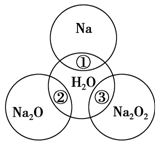 如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g,忽略溶液中溶剂的变化.完成下列题目.
如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g,忽略溶液中溶剂的变化.完成下列题目.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.16mol | B. | 0.21mol | C. | 0.30mol | D. | 0.48mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏操作时,冷凝管中冷却水应低进高出 | |
| B. | 萃取操作时,必须选择密度比水大的萃取剂 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 蒸发操作时,不能等到蒸发皿中水分完全蒸干后才停止加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com