
| A. | 稀硫酸 | B. | 氢氧化钠溶液 | C. | 稀硝酸 | D. | 浓硝酸 |
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
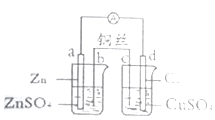
| A. | 电路中电子的流动方向:a-d-CuSO4(aq)一c一b | |
| B. | 该原电池原理:Zn+CuSO4═ZnSO4+Cu | |
| C. | c电极质量减少量等于d电极质量增加量 | |
| D. | d电极反应:Cu2++2e-=Cu,反应后CuSO4溶液浓度下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14gC8H16中的共用电子对数为3NA | |
| B. | 1mol苯中的碳碳双键数目为3NA | |
| C. | 1mol 二肽中含有的肽键数目为2NA | |
| D. | 30g甲酸甲酯与甲醛的混合物完全燃烧,生成的CO2的分子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 玻璃仪器 |
| A | 配制一定质量分数的NaCl溶液 | 胶头滴管、量筒、烧杯、玻璃棒 |
| B | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 |
| C | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 |
| D | 实验室用浓氨水和生石灰制备氨气 | 长颈漏斗、烧杯、玻璃棒 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下是气体 | B. | 能使溴的四氯化碳溶液褪色 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 在一定条件下能够聚合生成聚乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2Br→CH3CH2OH→CH2=CH2$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| B. | CH3CH2Br$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| C. | CH3CH2Br→CH2=CH2 $\stackrel{HBr}{→}$CH2BrCH3$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| D. | CH3CH2Br→CH2=CH2 $\stackrel{Br_{2}}{→}$CH2BrCH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮的重要化合物,如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等在生产、生活中具有重要作用.
氮的重要化合物,如氨(NH3)、肼(N2H4)、三氟化氮(NF3)等在生产、生活中具有重要作用.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com