
【题目】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
⑴氧化剂是_______________ , 还原剂是________________。
⑵氧化剂和还原剂的分子个数比___________________________。
⑶当有68克氨气参加反应时,被氧化的物质为_____________克, 生成还原产物为_________克。
【答案】 Cl2 NH3 3:2 17 160.5
【解析】(1)据反应8NH3+3Cl2=6NH4Cl+N2,反应中氯元素化合价从0价变化为-1价,化合价降低做氧化剂,氮元素化合价从-3价变化为0价,化合价升高做还原剂,故氧化剂是Cl2,还原剂是NH3;(2)反应8NH3+3Cl2=6NH4Cl+N2,氯气做氧化剂,氨气做还原剂,氧化产物为N2;3molCl2氧化2molNH3,得到1mol氧化产物N2,起还原剂作用的氨气2molNH3,物质的量之比等于分子个数比,所以氧化剂和还原剂的分子个数比为3:2;(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当8mol氨气反应时,被氧化的物质氨气为2mol,生成的还原产物氯化铵6mol,当有68克氨气,为![]() =4mol,参加反应时,被氧化的物质为1mol氨气,质量为17g;生成还原产物为3 mol氯化铵,质量为3 mol×53.5g=160.5g。
=4mol,参加反应时,被氧化的物质为1mol氨气,质量为17g;生成还原产物为3 mol氯化铵,质量为3 mol×53.5g=160.5g。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】I.磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素位于元素周期表第_______周期______族。AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为____________。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:________
□CuSO4+□PH3+□H2O═□Cu3P↓+□H3PO4+□H2SO4
(3)工业制备PH3的流程如图所示。

①黄磷和烧碱溶液反应的化学方程式为_________,次磷酸的化学式为____________,次磷酸属于___________(填“一”“二”或“三”)元酸。
②若起始时有1molP4参加反应,则整个工业流程中共生成 ______ mol PH3.(不考虑产物的损失)
II.某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。
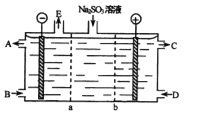
①a表示__________离子交换膜(填“阴”或“阳”)。A-E分别代表生产中的原料或产品。其中C为硫酸,则A表示_____________。E表示___________________。
②阳极的电极反应式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是
A. 含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
B. ![]() 的溶液中:Na+、K+、AlO2-、CO32-
的溶液中:Na+、K+、AlO2-、CO32-
C. 在pH=1的溶液中:K+、Al3+、SO42、F
D. 由水电离的c(H+)=10-14 mol·L-1的溶液中:K+、Na+、Ca2+、HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列十种物质:①H2O,②Cu,③NO,④Fe2O3,⑤稀硫酸,⑥氢氧化钡,⑦饱和FeCl3溶液,⑧氨水,⑨稀硝酸,⑩硫酸铝。根据上述提供的物质,回答下列问题:
(1)属于纯净物的是__________(填序号),属于电解质的是__________(填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH===H2O,则该反应的化学方程式为___________________________________________________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________________。
(4)实验室配制245 mL 0.5 mol/L的硫酸铝溶液,从配制好的溶液中取出100 mL,其中含有的![]() 的数目为_______(设NA为阿伏加德罗常数的值)。
的数目为_______(设NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
A. 某离子第三层上和第二层上的电子数均为第一层的4倍
B. Cl-的结构示意图:
C. 某物质的焰色反应为黄色,某物质一定为钠的化合物
D. 14C和14N的质量数相等,互称为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的结构简式为 CH2=CH-C≡C![]() ,下列有关其几何结构的说法正确的是( )
,下列有关其几何结构的说法正确的是( )
A. 所有碳原子不可能在同一平面上 B. 有4个碳原子在同一直线上
C. 有5个碳原子在同一直线上 D. 有6个碳原子在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X含有Ba2+、Al3+、NH![]() 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO![]() 、SO
、SO![]() 、SO
、SO![]() 、
、
Cl-、NO![]() 中的一种或几种,取该溶液进行实验,实验内容如下:
中的一种或几种,取该溶液进行实验,实验内容如下:
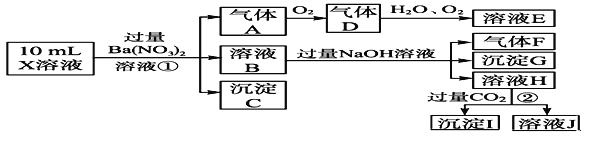
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是_____________________________________;
(2)写出有关离子方程式:
步骤①中生成A__________________;步骤②生成沉淀I__________________。
假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,若而沉淀C物质的量大于0.07 mol,溶液X中还一定含有的离子是______;若而沉淀C物质的量小于0.07 mol,溶液X中还一定含有的离子是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 在标准状况下,1mol水的体积是22.4L
B. 1molH2所占的体积约为22.4L
C. 在标准状况下,NA个分子所占的体积约为22.4L
D. 在标准状况下,1molNH3和CO混合气体所占的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关实验的说法中正确的是
A. 除去铁粉中的铜粉,加入足量浓硫酸加热反应后进行过滤
B. 不用任何其他试剂就可以鉴别NaOH溶液和Al2(SO4)3溶液
C. 制备Fe(OH)3胶体时,通常是将Fe(OH)3固体溶于沸水中
D. 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com