

分析 利用主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3的废金属屑制取新型高效水处理剂Na2FeO4,首先利用铝及其氧化物的两性性质用NaOH溶液溶解后再过滤除去,再用稀硫酸溶液滤渣,得到含有Fe2+、Fe3+的混合溶液并过虑除去铜,副产品Cu可以用热的稀硫酸并通氧气的情况下溶解得到硫酸铜溶液,滤液可通过氧化使溶液里只存在Fe3+,然后滴加NaOH溶液得到Fe(OH)3沉淀,再将经过过滤洗涤得到的Fe(OH)3固体溶解在NaOH和NaClO的混合溶液里可制目标产物;
(1)Al和Al2O3都有两性,加入过量的NaOH溶液,可溶解铝、氧化铝得到可溶性的偏铝酸钠溶液,通过过滤可除去;
(2)步骤Ⅱ在用稀硫酸溶解氧化铁生成硫酸铁,同时混合物中的铁会还原硫酸铁生成硫酸亚铁;
(3)铜能溶解在不断通氧气的热的稀硫酸中得到硫酸铜溶液,反应中氧气作氧化剂,还原产物为水,发生的化学方程式为2Cu+2H2SO4+O2=2CuSO4+2H2O,再改写成离子方程式;
(4)①溶液中亚铁离子被氧化为Fe3+,双氧水在反应中氧元素的化合价从-1价降低到-2价,得到1个电子,因此发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,由此可根据消耗的过氧化氢的质量,通过电子守恒进行计算;
②铁元素的化合价从+3价升高到+6价失去3个电子,次氯酸钠中氯元素的化合价从+1价降低到-1 价,得到2个电子.因此根据电子得失守恒可知还原剂与氧化剂的物质的量之比=2:3;根据原子守恒可知,反应中还有水生成,依据原子守恒配平书写化学方程式.
解答 解:(1)利用Al和Al2O3和Fe2O3的两性,用过量的NaOH溶液除去废金属屑中的Al和Al2O3发生反应的化学方程式为2Al+2H2O+2NaOH═2NaAlO2+3H2↑、Al2O3+2NaOH═2NaAlO2+H2O,故答案为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑、Al2O3+2NaOH═2NaAlO2+H2O;
(2)氧化铁溶于硫酸生成硫酸铁,同时混合物中的铁会还原硫酸铁生成硫酸亚铁,反应的离子方程式:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(3)铜溶解在不断通氧气的热的稀硫酸中得到硫酸铜溶液,发生反应的离子方程式为2Cu+O2+4H+═2Cu2++2H2O,故答案为:2Cu+O2+4H+═2Cu2++2H2O;
(4)①液中亚铁离子的物质的量是1000amol,生成氢氧化铁失去1000amol电子.双氧水在反应中氧元素的化合价从-1价降低到-2价,得到1个电子,因此1mol双氧水在反应中得到2mol电子.设需要双氧水溶液的质量是m,则根据电子得失守恒可知$\frac{m×25%}{34g/mol}$×2=1000amol,解得m=68000ag=68akg,故答案为:68a;
②铁元素的化合价从+3价升高到+6价失去3个电子,次氯酸钠中氯元素的化合价从+1价降低到-1 价,得到2个电子.因此根据电子得失守恒可知还原剂与氧化剂的物质的量之比=2:3;根据原子守恒可知,反应中还有水生成,依据原子守恒配平书写化学方程式,反应的化学方程式为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O,故答案为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O.
点评 本题考查物质的制备方案的设计,题目难度中等,解答本题时注意把握题给信息,学习中注重知识迁移能力的培养.


科目:高中化学 来源: 题型:选择题
| A. | 生石灰用作食品抗氧化剂 | |
| B. | Cl2+2Br-═2Cl-+Br2、Zn+Cu2+═Zn2++Cu均为单质被还原的置换反应 | |
| C. | 将KI和FeCl3溶液在试管中混合后,加入CCl4振荡、静置,下层溶液显紫红色,氧化性:Fe3+>I2 | |
| D. | 用含硅胶,铁粉的透气小袋与食品一起密封包装,这个过程不涉及化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 选用酒精作为萃取剂从碘水中萃取碘 | |
| B. | 蒸发操作时,待蒸发皿中的水分完全蒸干后再停止加热 | |
| C. | 在做蒸馏实验时,冷凝器中的水流方向应该与馏分的流动方向相反 | |
| D. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| E. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶中液面下,但不能接触瓶底 | |
| F. | 分液漏斗使用前不需检查是否漏水,但需要用蒸馏水洗涤2-3次 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从组成上来说,Na2SO4 是钠盐、硫酸盐、正盐 | |
| B. | 氧化物不是碱性氧化物就是酸性氧化物 | |
| C. | 非金属氧化物一定是酸性氧化物 | |
| D. | 不含杂质的盐酸是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
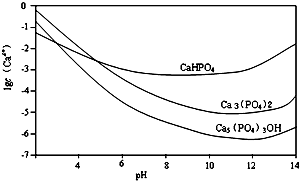 羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料.其常用的制备方法有两种:
羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料.其常用的制备方法有两种:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com