
| A. | 苯酚能与NaOH溶液反应,而己醇不能 | |
| B. | 乙烯可发生加成反应,而乙烷不能 | |
| C. | 苯酚能与浓溴水反应,而苯不可以 | |
| D. | 丙酮(CH3COCH3)分子中的氢原子比乙烷分子中的氢原子更易被卤原子取代 |
分析 A、-OH连接的烃基不同;
B、乙烯与乙烷的官能团不同;
C、酚-OH影响苯环;
D、丙酮(CH3COCH3)分子中的氢原子更易被卤素原子取代说明羰基与羟基对氢原子产生了影响.
解答 解:A、在苯酚中,由于苯环对-OH的影响,酚羟基具有酸性,对比乙醇,虽含有-OH,但不具有酸性,能说明上述观点,故A不选;
B、乙烯与乙烷的官能团不同,体现官能团对性质的影响,不能利用上述观点解释,故B选;
C、酚-OH影响苯环,则苯的性质不如苯酚活泼,苯酚中苯环上的H易取代,可利用上述观点解释,故C不选;
D、丙酮(CH3COCH3)分子中的氢原子比乙烷分子中氢原子更易被卤素原子取代,说明羰基与羟基对氢原子产生了影响,能由此规律解释,故D不选;
故选B.
点评 本题考查有机物结构与性质关系、原子团的相互影响等,把握原子之间相互影响及官能团对性质影响的差别为解答的关键,题目难度不大,注意基础知识的把握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
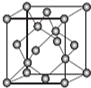 AIN是重要的半导体材料,Ga(镓)、P、As(砷)都是形成化合物半导体材料的重要元素.
AIN是重要的半导体材料,Ga(镓)、P、As(砷)都是形成化合物半导体材料的重要元素.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通常用小黑点来表示电子的多少,黑点密度大,电子数目大 | |
| B. | 黑点密度大小,表示单位体积内电子出现的机会多少 | |
| C. | 通常用小黑点来表示电子绕核作高速圆周运动 | |
| D. | 电子云图是对运动无规律性的描述 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
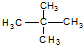 和
和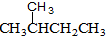 ⑧CH4和CH3CH3
⑧CH4和CH3CH3查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前2 s 的平均速率v(CO)=0.080mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(Cl2)=“0.11“mol•L-1,则反应的△H<0 | |
| C. | T K时起始向容器中充入0.9 mol COCl2、0.10 mol Cl2和0.10 mol CO,反应达到平衡前v正>v逆 | |
| D. | T K时起始向容器中充入1.0 mol Cl2和0.9 mol CO,达到平衡时,Cl2的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑨ | ⑩ | ||
| 4 | ② | ④ |
 ,该物质中含有的化学键类型为离子键与共价键(或非极性键);
,该物质中含有的化学键类型为离子键与共价键(或非极性键);查看答案和解析>>
科目:高中化学 来源: 题型:解答题
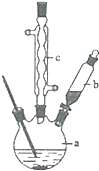 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要 +H2O+H2SO4$\stackrel{100-130℃}{→}$
+H2O+H2SO4$\stackrel{100-130℃}{→}$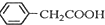 +NH4HSO4
+NH4HSO4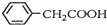 +Cu(OH)2→(
+Cu(OH)2→(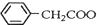 )2Cu+H2O
)2Cu+H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com