
为了消除氮的氧化物(NOx)对大气的污染,工业上通常利用反应NOx+NH3→N2+H2O来保护环境,现有NO2和NO的混合气体3L,可用3.5L NH3恰好使其完全转化为N2,则混和气体中NO2和NO的气体之比为( )
A.1:4 B.1:1 C.2:1 D.3:1
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A.硫酸工业尾气必须回收,净化处理,主要是为了充分利用原料
B.所谓“酸雨”,主要指含有硫的氧化物和氮的氧化物的雨水
C.大气中大量的SO2来源于煤和石油的燃烧以及金属矿石的冶炼
D.消除大气污染的主要方法之一是减少污染物的排放
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省海门市高二下学期期末教学质量调研化学试题 题型:填空题
氮是地球上极为丰富的元素。
(1)N2是大气的主要成分之一,由于分子中键能很大,所以性质稳定。已知N≡N的键能为946 kJ·mol-1,N—N单键的键能为193 kJ·mol-1。
计算:N2分子中“π”键的键能约为 ;
结论:N2分子中“σ”和“π”键的稳定性 。
(2)氮的氧化物是大气污染物之一。为了消除污染,科研人员设计了同时消除二氧化硫和氮的氧化物的方法,其工艺流程如下: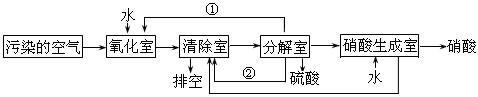
其中清除室、分解室发生的反应如下:
清除室:NO + NO2 = N2O3 N2O3 + 2H2SO4 = 2NOHSO4 + H2O
分解室:4NOHSO4 + O2 + 2H2O = 4H2SO4 + 4NO2
回答下列问题:
Ⅰ.①和②分别为(写化学式) 、 ;
Ⅱ.氧化室发生的反应是 ;
(3)金属氮化物是一类重要的化学物质,有着特殊的用途。某金属离子(M+)与N3—形成的晶体结构如右图所示。其 中M+中所有电子正好充满K、L、M三个电子层,它M+的符号是 ,与同一个N3-相连的M+有 个。
中M+中所有电子正好充满K、L、M三个电子层,它M+的符号是 ,与同一个N3-相连的M+有 个。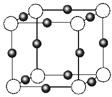
(4)NH3既是重要的工业产品,又是主要的工业原料。以NH3为原料生产硝酸铵的过
程如下: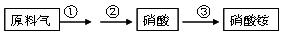
其中反应②为:4NO+3O2+2H2O=4HNO3 原料气为氨气和空气的混合物,假设空气中氧气的体积分数为0.2。
Ⅰ.写出反应①的化学方程式 。若不考虑副反应且各步反应均完全,生产过程中原料气中的氨气(不包含第③步被硝酸吸收的氨气)和空气中氧气恰好全部转化为硝酸,则原料气中制备硝酸的氨气和氧气的体积比为 。
Ⅱ.若实际生产中,反应①中氨的转化率(或利用率)为70%,反应②中NO的转化率为90%,反应③中氨和硝酸均完全转化。则生产硝酸的氨气占所用氨气总量的体积分数为多少?(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2010-2011学年甘肃省高三上学期第三次月考化学试卷 题型:选择题
下列说法中,不正确的是
A.硫酸工业尾气必须回收,净化处理,主要是为了充分利用原料
B.所谓“酸雨”,主要指含有硫的氧化物和氮的氧化物的雨水
C.大气中大量的SO2来源于煤和石油的燃烧以及金属矿石的冶炼
D.消除大气污染的主要方法之一是减少污染物的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
为了消除氮的氧化物(NOx)对大气的污染,工业上通常利用反应NOx+NH3→N2+H2O来保护环境,现有NO2和NO的混合气体6L,可用7L NH3恰好使其完全转化为N2,则混合气体中NO2和NO的气体之比为
![]() A.1:4 B.1:
A.1:4 B.1:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com