
| A、C2H5OH C3H7OH |
| B、C3H7OH CH3OH |
| C、CH3OH C2H5OH |
| D、C3H7OH C4H9OH |
| m |
| n |
| 0.224L |
| 22.4L/mol |
| 0.92g |
| 0.02mol |


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
| A、用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | ||||
B、用铜为电极电解饱和食盐水:2Cl-+2H2O
| ||||
| C、FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | ||||
| D、Ba(OH)2溶液中滴加过量NaHSO4:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
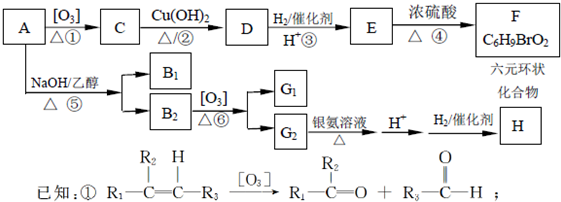
 )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下:| O2/Cu |
| △ |
| C |
| 一定条件 |
| (1)[Ag(NH3)2]OH,△ |
| (2)H+ |
| F |
| 浓H2SO4△ |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2O3、Al2O3 |
| B、Fe2O3 |
| C、Fe (OH)2、Al (OH)3 |
| D、Fe (OH)3、Al (OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
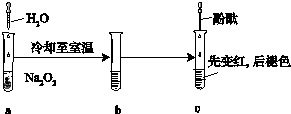 某化学小组进行Na2O2与水反应的实验,如图所示,该小组对试管c中红色褪去的原因进行探究.
某化学小组进行Na2O2与水反应的实验,如图所示,该小组对试管c中红色褪去的原因进行探究.| 实验 | 操作 | 现象 | 结论 |
| 1 | 向少量H2O2中滴加2滴酚酞,放置一段时间,再加入NaOH溶液至pH=12 | 加入NaOH后,无色溶液先变红,后褪色 | ① |
| 2 | 向少量 NaOH溶液(pH=14)中滴加2滴酚酞;再加适量稀盐酸至溶液 pH=12 | 溶液先变红,后褪色;加盐酸后,又出现红色,且不褪色 | |
| 3 | 向Na2O2与水反应后的溶液(pH=14)中滴加2滴酚酞;再加适量稀盐酸至溶液 pH=12 … | ② … | 溶液pH大于13时,NaOH使变红的溶液褪色;pH在8~13时,NaOH和H2O2共同作用使溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com