
ijЩ��ѧ���ļ����������±���ʾ��kJ��mol��1����
| �� | H��H | Br��Br | I��I | Cl��Cl | H��Cl | H��I[ | H��Br |
| ���� | 436 | 193 | 151 | 247 | 431 | 299 | 356 |
�����ϱ������ݣ����н�����ȷ����
A.��1mol Cl2�ֽ�Ϊ��̬ԭ��ʱ����Ҫ�ų�247 kJ����
B.�ɱ������л�ѧ���γɵĵ��ʷ����У����ȶ�����H2 ,�γɵĻ���������У���ȶ�����HI
C.��һ�������£�1mol H2 ��������Cl2 ��Br2 ��I2 �ֱ�Ӧ���ų������ɶൽ�ٵ���I2 > Br2> Cl2
D.Ԥ��1mol H2 ������F2 ��ȼ�ձ���Cl2�з�����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| 1 |
| 2 |
| 1 |
| 2 |
| ��ѧ�� | C-C | C-H | H-H | C-O | C��O | H-O |
| ����/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 3 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| ��ѧ�� | C-C | C-H | H-H | C-O | C��O��CO�� | H-O |
| ����/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 1 |
| 2 |
| 1 |
| 2 |
| ��ѧ�� | C-C | C-H | H-H | C-O | C��O | H-O |
| ����/kJ?mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 3 |
| 2 |
| c(CH3OH) |
| c(CO)��c2(H2) |
| c(CH3OH) |
| c(CO)��c2(H2) |
| 3 |
| 2 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ѧ�� | N��N | H-H | N-H |
| ����kJ?mol-1 | 946 | 436 | 390 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���㽭ʡ������ʮУ�����������ѧ���ڳ����Ի�ѧ�Ծ����������� ���ͣ������
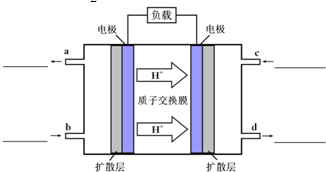
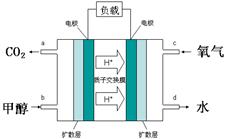
��12�֣��״���һ�����͵���������ȼ�ϣ���ҵ�Ͽ�ͨ��CO��H2�����Ʊ��״����÷�Ӧ���Ȼ�ѧ����ʽΪ��CO(g)+2H2(g) CH3OH(g) �SH ��֪ijЩ��ѧ���ļ����������±���
CH3OH(g) �SH ��֪ijЩ��ѧ���ļ����������±���
| ��ѧ�� | C��C | C��H | H��H | C��O | C��O | H��O |
| ����/kJ��mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| ��Ӧʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 |
| ѹǿ/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com