
分析 (1)根据醋酸钠固体对平衡CH3COOH?CH3COO-+H+的影响分析;
(2)醋酸根离子结合水电离的氢离子生成醋酸,反应是可逆的;醋酸根离子的水解是吸热反应;
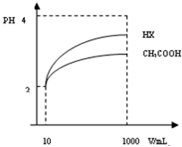
(3)醋酸钠溶液中物质的量浓度越大,水解程度越越小,但是溶液中氢氧根离子浓度越大,溶液的PH越大;
(4)将等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合后,恰好生成CH3COONa,为强碱弱酸盐,溶液呈碱性;
(5)pH<7溶液显示酸性,溶液中氢离子大于氢氧根离子浓度,醋酸根离子浓度大于钠离子浓度;
(6)pH=3的HA溶液中氢离子浓度和pH=11的NaOH溶液中的氢氧根离子相等,醋酸是弱电解质,氢氧化钠是强电解质,根据这些对选项进行判断;
(7)根据离子的浓度和氢氧根离子浓度,计算出各种离子的离子积,然后根据KSP[Mg(OH)2]=1.8×10-11、KSP[Zn(OH)2]=1.2×10-17、KSP[Cd(OH)2]=2.5×10-14进行判断是否生成沉淀;
(8)根据10mL 0.5mol•L-1盐酸溶液,计算出氢离子的物质的量浓度,溶液稀释,氢离子物质的量不变,计算出稀释后溶液中氢离子浓度;盐酸溶液中水电离的氢离子等于溶液中氢氧根离子的浓度.
解答 解:(1)因醋酸钠固体电离产生CH3COO-,c(CH3COO-)增大,使的平衡CH3COOH?CH3COO-+H+逆向移动,C(H+)减小,C(CH3COOH)增大,所以C(H+)与C(CH3COOH)的比值减小,故答案为:减小;
(2)醋酸钠水解的离子方程式为:CH3COO-+H2O?CH3COOH+OH-,该反应是吸热反应,温度升高,溶液中氢氧根离子浓度增大,
故答案为:CH3COO-+H2O?CH3COOH+OH-;增大;
(3)由于醋酸钠溶液中,醋酸钠的浓度越大,水解程度越小,但是溶液中的氢氧根离子的物质的量浓度反而越大,溶液的PH越大,所以m小于n,a大于b,
故答案为:小于;大于;
(4)醋酸为弱电解质,将等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合后,恰好生成CH3COONa,为强碱弱酸盐,溶液呈碱性,c(OH-)>c(H+),溶液中存在:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),则c(Na+)>c(CH3COO-),
故答案为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
(5)由于溶液的PH小于7,溶液中氢离子物质的量浓度大于氢氧根离子的浓度,氢离子主要是醋酸电离的,所以醋酸根离子浓度大于钠离子浓度,c(Na+) 大于c(CH3COO-)(
故答案为:大于;
(6)A、若反应后溶液呈中性,溶液中氢离子浓度=氢氧根离子浓度=1×10-7mol•L-1c(H+)+c(OH-)=2×10-7mol•L-1,故A说法正确;
B、醋酸是弱电解质部分电离,醋酸的浓度大于氢氧化钠的浓度,若V1=V2,反应后溶液pH一定小于7,故B说法错误;
C、若反应后溶液呈酸性,由于醋酸浓度大于氢氧化钠浓度,则V1≤V2,故C说法错误;
D、若反应后溶液呈碱性,由于V1=V2溶液显示酸性,所以V1一定小于V2,故D说法正确;
故选AD,
故答案为:AD;
(7)溶液中氢氧根离子浓度是:[OH-]=2.2×10-5mol•L-1,根据[M2+][OH-]2=5×10-12(mol•L-1)3,
由于5×10-12小于KSP[Mg(OH)2]=1.8×10-11,没有氢氧化镁沉淀生成,
由于5×10-12大于KSP[Zn(OH)2]=1.2×10-17,有氢氧化锌沉淀生成,
由于5×10-12大于KSP[Cd(OH)2]=2.5×10-14,有Cd(OH)2沉淀生成,
故答案为:Cd2+、Zn2+;
[H-]=2.2×10-5mol•L-1
[M2+][OH-]2=5×10-12(mol•L-1)3
5×10-12小于KSP[Mg(OH)2]=1.8×10-11
5×10-12大于KSP[Zn(OH)2]=1.2×10-17
5×10-12大于KSP[Cd(OH)2]=2.5×10-14
(8)稀释后溶液中的氢离子浓度是:c(H+)=$\frac{0.5mol/L×0.01L}{0.5L}$=0.01mol/L,由于盐酸溶液中,水电离的氢离子浓度等于溶液中的氢氧根离子的浓度,该溶液中由水电离出的c(H+)=1×10-12,
故答案为:1×10-12.
点评 本题考查弱电解质的电离平衡、盐类水解、离子浓度比较、溶液PH值的判断等,涉及的题目容量较大,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 22.4 L乙烯中含有的分子数为NA | |
| B. | 0.1 L 0.1 mol/L的CH3COOH溶液中含有的分子数为0.01 Na | |
| C. | 含0.1 mol H2O2的水溶液跟MnO2充分作用,反应过程中转移的电子总数0.1Na | |
| D. | 1 mol HCl气体中的粒子数与0.5 mol/L盐酸中溶质粒子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol H2 | B. | 0.5 mol NH3 | ||
| C. | 6.02×1023个的CH4分子 | D. | 0.3 mol H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X为0.2 mol•L-1 | |
| B. | Y为0.1 mol•L-1 | |
| C. | Z为0.4 mol•L-1 | |
| D. | Z为0.1 mol•L-1时,Y为0.15 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、AlO2-、Cl- | B. | Na+、NH4+、S2- | C. | H+、Cl-、Fe2+ | D. | Mg2+、Ba2+、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 为测定硫酸钠晶体的化学式,取样品32.2g配成100mL溶液,再滴入5mol/L氯化钡溶液,当滴入20mL时恰好不再产生沉淀,试通过计算写出硫酸钠晶体的化学式.
为测定硫酸钠晶体的化学式,取样品32.2g配成100mL溶液,再滴入5mol/L氯化钡溶液,当滴入20mL时恰好不再产生沉淀,试通过计算写出硫酸钠晶体的化学式.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的稳定性H2T<H2R | B. | M与T形成的化合物具有两性 | ||
| C. | 单质与稀盐酸反应的快慢为L>Q | D. | L2+与R2-的核外电子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com