
【题目】K3[Fe(C2O4)3](三草酸合铁酸钾)可用于摄影和蓝色印刷。工业上制备K3[Fe(C2O4)3]的反应原理如下:
氧化:6FeC2O4+3H2O2+6K2C2O4═4K3[Fe(C2O4)3]+2Fe(OH)3
转化:2Fe(OH)3+3K2C2O4+3H2C2O4═2K3[Fe(C2O4)3]+6H2O
(1)制备1mol三草酸合铁酸钾至少需要H2O2的物质的量为___。
(2)制备过程中需防止草酸被H2O2氧化,写出草酸被H2O2氧化的化学方程式:___。
(3)K3[Fe(C2O4)3]·xH2O(三草酸合铁酸钾晶体)是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组进行了如下实验:
①称量9.820g三草酸合铁酸钾晶体,配制成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,滴加KMnO4溶液至C2O42-全部转化成CO2时,恰好消耗24.00mL0.1000molL-1KMnO4溶液。C2O42-被全部转化的标志是___。
③计算该晶体的化学式,并写出计算过程。___
【答案】0.5mol H2C2O2+H2O2=2CO2+2H2O 溶液由无色转变为紫红色,且30秒内不再变化 K3[Fe(C2O4)3]·3H2O
【解析】
(1)由氧化及转化反应可知,存在3H2O2~6K3[Fe(C2O4)3];
(2)草酸被H2O2氧化生成二氧化碳和水;
(3)②C2O42﹣被全部转化,高锰酸钾过量,溶液由无色变为紫色;
③由Fe元素守恒计算25mL溶液中n(Fe3+),然后计算9.82g草酸合铁酸钾晶体中n(Fe3+),再根据电荷守恒计算n(K+),晶体中m(H2O)=9.82g﹣m(K+)﹣m(Fe3+)﹣m(C2O42﹣),进而计算n(H2O),从而确定其化学式。
(1)由氧化及转化反应可知,存在3H2O2~6K3[Fe(C2O4)3],则制备1mol三草酸合铁酸钾至少需要H2O2的物质的量为1mol×![]() =0.5mol;
=0.5mol;
(2)草酸被H2O2氧化的化学方程式为H2C2O2+H2O2=2CO2+2H2O;
(3)C2O42﹣被全部转化的标志是为溶液由无色转变为紫红色,且30秒内不再变化;
(4)消耗KMnO4的物质的量为0.1000mol/L×0.024L=0.0024mol,由5C2O42﹣+2MnO4﹣+16H+=2Mn2++8H2O+10CO2↑可知,n(C2O42﹣)=0.024mol×![]() =0.006mol,250mL原溶液中C2O42﹣的物质的量为0.006mol×10=0.06mol,则n[K3Fe(C2O4)3]=0.06mol×
=0.006mol,250mL原溶液中C2O42﹣的物质的量为0.006mol×10=0.06mol,则n[K3Fe(C2O4)3]=0.06mol×![]() =0.02mol,m[K3Fe(C2O4)3]=n[K3Fe(C2O4)3]M=0.02×437=8.74g,m(H2O)=9.82﹣8.74=2.28=1.08g,n(H2O)=
=0.02mol,m[K3Fe(C2O4)3]=n[K3Fe(C2O4)3]M=0.02×437=8.74g,m(H2O)=9.82﹣8.74=2.28=1.08g,n(H2O)=![]() =0.06ml,即0.02x=0.06,故x=3,则该晶体的化学式为K3[Fe(C2O4)33H2O]。
=0.06ml,即0.02x=0.06,故x=3,则该晶体的化学式为K3[Fe(C2O4)33H2O]。


科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中 使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀。

(1)物质A的化学式为 ________,F化学式为 ________;
(2)B和R在溶液中反应生成F的离子方程式为__________________________;
(3)H在潮湿空气中变成M的实验现象是________,化学方程式为______________;
(4)A和水反应生成B和C的化学方程式为__________________________
(5)印刷行业刻制印刷电路板(含有铜箔)时,要用W溶液中作为“腐蚀液”,写出该反应的离子方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
B | 向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
C | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
D | 向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl) >Ksp(AgI) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种航天器能量储存系统原理示意图。下列说法正确的是
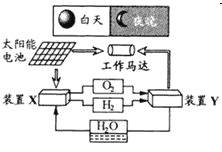
A. 该系统中只存在3种形式的能量转化
B. 装置Y中负极的电极反应式为:![]()
C. 装置X能实现燃料电池的燃料和氧化剂再生
D. 装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中溴元素以Br形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图所示:

(1)步骤①反应的离子方程式是____________________,步骤③反应的化学方程式是___________________。
(2)从理论上考虑,下列物质也能吸收Br2的是___________(填字母)。
A.NaOH B.FeCl2
C.Na2SO3 D.H2O
(3)步骤③中氧化剂是________,若反应中生成2 mol HBr,则消耗________mol SO2。
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包白色粉末,可能由NaCl、Na2CO3、Na2SO4中的一种或几种组成,为鉴别其成分进行如下实验(每步加入试剂都是足量的):
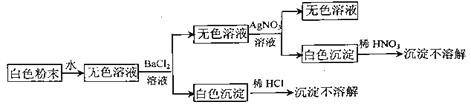
下列说法错误的是( )
A.粉末中一定含有NaClB.粉末中一定含有Na2SO4
C.粉末中一定不含Na2CO3D.粉末可能是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4 L氢气中含有2NA个中子
B. 0.1NA个氯化氢分子占有体积为2.24 L
C. 2克金属钙变成钙离子时失去的电子数为0.1NA
D. 50 mL 0.1 mol·L-1H2SO4溶液中含有H+数为0.005NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A. 1 mol![]() 所含的质子数和电子数都为10NA
所含的质子数和电子数都为10NA
B. NA个微粒就是6.02×1023个微粒
C. 0.1 mol硫酸中含有的原子总数为0.7NA
D. 1 mol CO所含电子数是28NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B分别为第三、四周期同一主族的不同元素的原子,它们原子核内的质子数等于中子数。
①若A为第ⅡA族元素,其质量数为x,则B的质子数为y。
②若A为第ⅣA族元素,其质子数为m,则B的质量数为n。
则y和n的值分别是
A. (![]() +18)、(2m+18)B. (
+18)、(2m+18)B. (![]() +8)、(2m+18)
+8)、(2m+18)
C. (![]() +8)、(2m+36)D. (
+8)、(2m+36)D. (![]() +18)、(2m+36)
+18)、(2m+36)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com