
| A. | 2s | B. | 5f | C. | 2d | D. | 3px |
分析 根据第一层(K层)上只有1S亚层,第二电子层(L层)只有2s和2p亚层,第三电子层(M层)只有3s、3p和3d亚层,第四电子层(N层)只有4s、4p、4d和4f亚层,结合各能级含有的轨道分析,s能级只有1个轨道,p能级有3个轨道,d能级有5个轨道,f能级有7个轨道,注意不存在1p、2d、3f能级,结合选项符号能否指明确定的轨道进行判断.
解答 解:A.2s能级只有1个轨道,故2s可以表示原子轨道,故A不选;
B.第五能层含有5s、5p、5d、5f能级,所以存在5f能级,故B不选;
C.第二能层含有2s、2p两个能级,所以不存在2d能级,故C选;
D.第三能层含有3s、3p、3d三个能级,所以存在3p能级,3p能级含有3个轨道,3个轨道相互垂直,3px表示为x轴上的轨道,故D不选;
故选C.
点评 本题考查了能层中的能级排布,题目难度不大,从能层数与能级数之间的关系分析解答,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:选择题
 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )| A. | 最简单氢化物的稳定性:R>Q>X;R>T>X | |
| B. | 五种元素中Z的活动性最弱,T的氧化物对应水化合物酸性最强 | |
| C. | Q单质能从溶液中置换出X单质,R单质能从溶液中置换出T单质 | |
| D. | X阴离子和T阴离子相比,半径:X阴离子的大;还原性:T阴离子的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 据图可知,阳极反应式为2SO42--4e-=2SO3↑+O2↑ | |
| B. | 阳极失去2mol电子时,理论上可以得到11.2L氧气 | |
| C. | SO2在阴极与O2反应生成硫酸根,则方程式为SO2+O2+2e-=SO42- | |
| D. | CO2不参与电极反应,净化器中CO2浓度升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
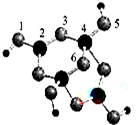 回答以下问题:
回答以下问题:| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
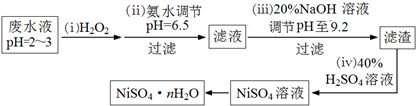
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铜分别溶于盐酸和醋酸 | |
| B. | 石灰石分别与硝酸和盐酸反应 | |
| C. | 硫酸铜溶液分别与氯化钡和氢氧化钡溶液反应 | |
| D. | 稀硫酸分别与碳酸钠、碳酸氢钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com