
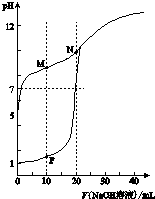
 温室下,用0.1mol•L-1NaOH溶液分别滴定体积均为20ml浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化图,下列说法不正确的是( )
温室下,用0.1mol•L-1NaOH溶液分别滴定体积均为20ml浓度均为0.1mol•L-1HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化图,下列说法不正确的是( )| A. | HX为弱酸 | |
| B. | M点c(HX)-c(X-)>c(OH-)-c(H+) | |
| C. | 将P点和N点的溶液为混合,呈酸性 | |
| D. | 向N点溶液中通入HCl至pH=7:c(Na+)>c(HX)=c(Cl-)>c(X-) |
分析 A.根据未滴定时0.1mol•L-1HCl和HX溶液的pH进行判断;
B.M点为等浓度NaX、HX混合溶液,且溶液呈碱性,说明X-的水解程度大于HX的电离程度,由物料守恒可知:2c(Na+)=c(X-)+c(HX),结合电荷守恒c(Na+)+c(H+)=c(X-)+c(OH-)判断;
C.P点溶液中NaCl、HCl物质的量相等,N点为NaX溶液,NaX物质的量为HCl的2倍,P、N点溶液混合后为NaCl、NaX、HX混合溶液,且溶液中NaX与HX的浓度相等,由于X-的水解程度大于HX的电离程度,呈碱性;
D.根据电荷守恒:c(Na+)+c(H+)=c(Cl-)+c(X-)+c(OH-),溶液pH=7,则c(Na+)=c(Cl-)+c(X-),由物料守恒可知c(Na+)=c(X-)+c(HX),联立可得c(HX)=c(Cl-),而溶液为NaCl、NaX、HX的混合溶液,相同浓度下X-的水解程度大于HX的电离程度,由于溶液为中性,则溶液中c(NaX)<c(HX).
解答 解:A.未滴定时,0.1mol•L-1HCl溶液pH为1,由图可知0.1mol/L HX溶液的pH>5,则HX弱酸,故A正确;
B.M点为等浓度NaX、HX混合溶液,且溶液呈碱性,说明X-的水解程度大于HX的电离程度,由物料守恒可知:2c(Na+)=c(X-)+c(HX),结合电荷守恒c(Na+)+c(H+)=c(X-)+c(OH-),联立可得:c(X-)+c(HX)+2c(H+)=2c(X-)+2c(OH-),整理得:c(HX)-c(X-)=2c(OH-)-2c(H+)>c(OH-)-c(H+),故B正确;
C.P点溶液中NaCl、HCl物质的量相等,N点为NaX溶液,NaX物质的量为HCl的2倍,混合后为NaCl、NaX、HX混合溶液,且溶液中NaX与HX的浓度相等,由于X-的水解程度大于HX的电离程度,呈碱性,故C错误;
D.根据电荷守恒:c(Na+)+c(H+)=c(Cl-)+c(X-)+c(OH-),溶液pH=7,则c(Na+)=c(Cl-)+c(X-),由物料守恒可知c(Na+)=c(X-)+c(HX),联立可得c(HX)=c(Cl-),而溶液为NaCl、NaX、HX的混合溶液,相同浓度下X-的水解程度大于HX的电离程度,由于溶液为中性,则溶液中c(NaX)<c(HX),故溶液中c(Na+)>c(HX)=c(Cl-)>c(X-),故D正确.
故选:C.
点评 本题考查盐类水解、弱电解质电离、离子浓度大小判断,关键是根据M点判断相同浓度下X-的水解程度大于HX的电离程度,难度较大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
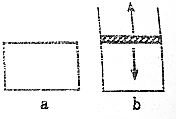 已知2N02?N2O4△H<0.将N02充入容易导热的材料制成的容器a和b中进行反应,a的容积保持不变,b的上盖可随容器内气体压强的改变而上下移动,以保持容器内外压强相等.当同温同压时,将等量的NO2充入“起始态”体积相同的容器a、b中,反应同时开始.
已知2N02?N2O4△H<0.将N02充入容易导热的材料制成的容器a和b中进行反应,a的容积保持不变,b的上盖可随容器内气体压强的改变而上下移动,以保持容器内外压强相等.当同温同压时,将等量的NO2充入“起始态”体积相同的容器a、b中,反应同时开始.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 实验目的 |
| (滴定前的所有操作正确,已略去) 步骤1: ①用碱式滴定管量取20.00mL的氨水放入锥形瓶中,滴入2滴甲基橙. ②用酸式滴定管取0.1000mol/L盐酸滴定氨水. ③当锥形瓶中的溶液由黄色变成橙色时,停止滴定,纪录数据. ④重复滴定操作2~3次. | 测定氨水的准确浓度 |
| 步骤2:用pH计测定氨水的pH. | 测定氨水中c(OH-)浓度 |
| 步骤3:通过实验数据计算氨水的电离常数K | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如图:
实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如图:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合溶液呈中性 | |
| B. | a≥b | |
| C. | 混合溶液中,c(A-)=c(Na+) | |
| D. | 混合液中水电离出c(OH-)大于该温度下纯水电离出c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 名称 | 相对密度 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醚 | ||||
| 苯甲醛 | 1.04 | -26 | 179.6 | 微溶 | 易溶 |
| 苯甲酸 | 1.27 | 122.1 | 249 | 25℃微溶,95℃可溶 | 易溶 |
| 苯甲醇 | 1.04 | -15.3 | 205.7 | 微溶 | 易溶 |
| 乙醚 | 0.71 | -116.3 | 34.6 | 不溶 | -- |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “静电除尘”、“汽车尾气的催化净化”都有利于提高空气质量 | |
| B. | 减少化石燃料的使用,有利于降低空气中PM2.5的含量 | |
| C. | 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质 | |
| D. | 医用酒精是用淀粉类植物发酵经蒸馏制成,浓度通常是75% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com