
分析 (1)氯气在70℃的NaOH溶液中能发生两个反应,产物除水外还有氯化钠、次氯酸钠和氯酸钠(NaClO3),其中反应之一为3Cl2+6NaOH═5NaCl+NaClO3+3H2O,则另一个反应是生成次氯酸钠的反应,方程式为:Cl2+2NaOH═NaCl+NaClO+H2O;
(2)根据氯守恒,2n(Cl2)=n(NaClO3)+n(NaClO)+n(NaCl),由此分析解答.
解答 解:(1)氯气在70℃的NaOH溶液中能发生两个反应,产物除水外还有氯化钠、次氯酸钠和氯酸钠(NaClO3),其中反应之一为3Cl2+6NaOH═5NaCl+NaClO3+3H2O,则另一个反应是生成次氯酸钠的反应,方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,故答案为:Cl2+2NaOH═NaCl+NaClO+H2O;
(2)根据氯守恒,2n(Cl2)=n(NaClO3)+n(NaClO)+n(NaCl)=0.8mol,所以n(Cl2)=$\frac{0.8mol}{2}$=0.4mol,答:参加反应的氯气的物质的量是0.4mol.
点评 本题考查氧化还原反应计算、根据方程式的计算等,难度较大,注意原子守恒和得失电子守恒法的利用.


科目:高中化学 来源: 题型:选择题
| A. | 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 | |
| B. | 若 2C(s)+O2(g)=2CO(g)△H=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol | |
| C. |  如图可表示水分解过程中的能量变化 | |
| D. | 已知: Ⅰ:对于反应:H2(g)+Cl2(g)=2HCl (g)△H=-a kJ/mol, Ⅱ:  且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为(a+b+c)kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤⑧⑨⑩ | B. | ②④⑥⑦ | C. | ②⑤⑦⑧⑩ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
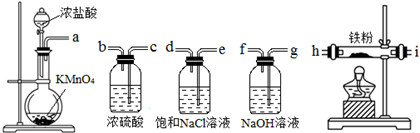
| A. | a-e-d-c-b-h-i-g | B. | a-d-e-c-b-h-i-g | C. | a-e-d-h-i-g-f-c | D. | a-b-c-d-e-f-g-h |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔沸点:SiO2>NaCl>S>CO2 | B. | 酸性:HNO2<HNO3;H3PO4<H2SO4 | ||
| C. | 还原性:H2S>HI>HBr>HCl | D. | 键长:C-H<N-H<O-H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2溶于水反应,反应转移电子数为nA | |
| B. | 56g晶体硅中含有硅分子数为2nA | |
| C. | 1 mol Cu和足量稀硝酸反应产生nA个NO分子 | |
| D. | 标准状况下,1.12 L NO与1.12 L O2的混合物中含有的原子数为0.2nA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸的电离 | B. | Ba(OH)2•8H2O晶体与NH4Cl晶体反应 | ||
| C. | 焦炭与二氧化碳气体发生的反应 | D. | Na与H2O反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com