
【题目】按要求回答下列问题:
(1)写出乙烯分子的电子式:________。
(2)写出(2﹣甲基﹣1,3﹣丁二烯)的结构简式_____________。
(3)立方烷 ![]() 的一氯代物有__________种,它的六氯代物有________种。
的一氯代物有__________种,它的六氯代物有________种。
(4)下列物质的沸点按由高到低的顺序排列正确的是________。
①CH3(CH2)2CH3 ②CH3(CH2)3CH3 ③(CH3)3CH ④(CH3)2CHCH2CH3
A.②④①③ B.④②①③ C.④③②① D.②④③①
(5)下列选项中互为同系物的是________;互为同分异构体的是________;属于同种物质的是________。
①O2和O3 ②1H、2H、3H ③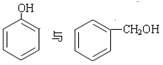 ④
④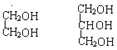 ⑤
⑤![]() ⑥戊烯和环戊烷 ⑦
⑥戊烯和环戊烷 ⑦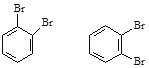
【答案】![]()
![]() 1 3 A ⑤ ⑥ ⑦
1 3 A ⑤ ⑥ ⑦
【解析】
(1)乙烯分子中碳原子之间以双键相连,碳剩余价键被H饱和,由此可写出电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)2﹣甲基﹣1,3﹣丁二烯,主链为1,3-丁二烯,在2号碳上含有一个甲基,其结构简式为:![]() ,故答案为:
,故答案为:![]() ;
;
(3)立方烷 ![]() 只有1种H,故其一氯代物有1种,它的六氯代物和二氯代物的数目是一样的,其二氯代物有两个氢原子在同一个面内相邻、相间2种,不同面内体对角线相对1种,共3种,则其六氯代物也为3种,故答案为:1;3;
只有1种H,故其一氯代物有1种,它的六氯代物和二氯代物的数目是一样的,其二氯代物有两个氢原子在同一个面内相邻、相间2种,不同面内体对角线相对1种,共3种,则其六氯代物也为3种,故答案为:1;3;
(4)①CH3(CH2)2CH3 ②CH3(CH2)3CH3 ③(CH3)3CH ④(CH3)2CHCH2CH3均为烷烃,相对分子质量越大,范德华力越大,沸点越高,即碳原子数越多,沸点越高,若碳原子数相同的烷烃,支链越多,熔沸点越低,②CH3(CH2)3CH3,④(CH3)2CHCH2CH3均为5个碳原子,而④有1个支链,②没有,①CH3(CH2)2CH3,③(CH3)3CH均为4个碳,①没有支链,③有1个支链,则沸点顺序由高到低的顺序为②④①③,A选项正确,故答案为:A;
(5)①O2和O3是同一种元素组成的不同种单质,属于同素异形体;
②1H、2H、3H的质子数相同,中子数不同,互为同位素;
③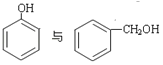 结构不相似,前者是酚,后者是醇,不是同系物;
结构不相似,前者是酚,后者是醇,不是同系物;
④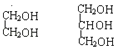 ,前者是二元醇,后者是三元醇,不是同系物;
,前者是二元醇,后者是三元醇,不是同系物;
⑤![]() 结构相似,且分子式相差2个—CH2,是同系物;
结构相似,且分子式相差2个—CH2,是同系物;
⑥戊烯和环戊烷分子式均为C5H10,但结构不同,属于同分异构体;
⑦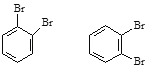 是同一物质;
是同一物质;
综上,互为同系物的是⑤,互为同分异构体的是⑥,属于同种物质的是⑦,故答案为:⑤;⑥;⑦。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】检验甲醛含量的方法有很多,其中银﹣Ferrozine法灵敏度较高。测定原理为甲醛把氧化银还原成Ag,产生的Ag与Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪(Ferrozine)形成有色配合物,通过测定吸光度计算出甲醛的含量。某学习小组类比此原理设计如下装置测定新装修居室内空气中甲醛的含量(夹持装置略去)。

已知:甲醛能被银氨溶液氧化生成CO2,氮化镁与水反应放出NH3,毛细管内径不超过1 mm。请回答下列问题:
(1)A装置中反应的化学方程式为___________,用饱和食盐水代替水制备NH3的原因是___________________。
(2)B中装有AgNO3溶液,仪器B的名称为________。
(3)银氨溶液的制备。关闭K1、K2,打开K3,打开______,使饱和食盐水慢慢滴入圆底烧瓶中,当观察到B中白色沉淀恰好完全溶解时,________。
(4)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K1,将滑动隔板慢慢由最右端抽到最左端,吸入1 L室内空气,关闭K1;后续操作是______________;再重复上述操作3次。毛细管的作用是__________。
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=1,再加入足量Fe2(SO4)3溶液,充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562 nm处测定吸光度,测得生成Fe2+1.12 mg,空气中甲醛的含量为____mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗是重要的半导体材料,应用于航空航天测控、光纤通讯等领域.一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如下:
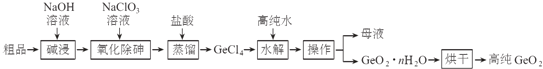
已知:①“碱浸”过程中的反应为:
GeO2+2NaOH=Na2GeO3+H2O
As2O3+2NaOH=2NaAsO2+H2O
②“蒸馏”过程中的反应为:Na2GeO3+6HCl=2NaCl+GeCl4+3H2O
③GeCl4的熔点为-49.5℃,AsCl3与GeCl4的沸点分别为130.2℃、84℃.
(1)锗的原子序数为32,锗在元素周期表中的位置为第 ______ 周期 ______ 族.
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应方程式为: ______ .
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是 ______ .
(4)工业上与蒸馏操作相关的设备有 ______
A.蒸馏釜 B.离心萃取机 C.冷凝塔 D.加压过滤机
(5)“水解”操作时发生的化学反应方程式为 ______ ,“水解”操作时保持较低温度有利于提高产率,其最可能的原因是 ______ (答一条即可).
(6)若1吨二氧化锗粗品(含杂质30%)经提纯得0.745吨的高纯二氧化锗产品,则杂质脱除率为 ______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核内中子数为N的R2+,质量数为A,则ng它的同价态氧化物中所含电子物质的量为( )
A.![]() (A+N-10)molB.
(A+N-10)molB.![]() (A-N+6)mol
(A-N+6)mol
C.(A-N+2)molD.![]() (A-N+8)mol
(A-N+8)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将0.1 mol·L-1 NaOH溶液逐滴滴入10 mL 0.1 mol·L-1 NH4HSO4溶液中,溶液的pH与NaOH溶液体积关系如图所示:
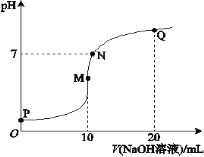
下列关系中,不正确的是
A.M点c(Na+)>c(![]() )
)
B.N点c(![]() )+c(Na+)=2c(
)+c(Na+)=2c(![]() -)
-)
C.Q点c(![]() )+c(NH3·H2O)=c(Na+)
)+c(NH3·H2O)=c(Na+)
D.M、N、Q三点中,水的电离程度M>N>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1934年,居里夫妇用![]() 粒子
粒子![]() 轰击
轰击![]() 得到一种自然界中不存在的磷元素的一种核素
得到一种自然界中不存在的磷元素的一种核素![]() :
:![]() ,开创了人造核素的先河。
,开创了人造核素的先河。
(1)下列有关说法正确的有______(填序号)。
A.![]() 的质子数是27 B.
的质子数是27 B.![]() 是一种电中性粒子
是一种电中性粒子
C.![]() 和
和![]() 互为同位素 D.P元素的相对原子质量为30
互为同位素 D.P元素的相对原子质量为30
(2)元素的化学性质主要取决于______(填序号)。
A.原子最外层电子数 B.原子核内中子数
C.原子核内质子数 D.原子质量数
(3)不同种元素的本质区别是______(填序号)。
A.原子的质子数不同 B.原子的中子数不同
C.原子的最外层电子数不同 D.原子的质量数不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为从固体混合物中分离X的两种方案,请根据方案1和方案2指出下列说法中合理的是( )

A. 可以选用方案1分离碳酸氢钠中含有的氯化铵
B. 方案1中的残留物应该具有的性质是受热易挥发
C. 方案2中加入的试剂一定能够与除X外的物质发生化学反应
D. 方案2中加入NaOH溶液可以分离出SiO2和Fe2O3混合物中的Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于浓硫酸特性的叙述不正确的是
A. 浓硫酸具有吸水性、脱水性和强氧化性等特性
B. 浓硫酸能吸收气体中的水蒸气,常作氨气、二氧化硫等气体的干燥剂
C. 浓硫酸可以吸收固体中的湿存水、结晶水合物中的结晶水
D. 在反应C12H22O11![]() 12C+11H2O,浓硫酸作脱水剂
12C+11H2O,浓硫酸作脱水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是_____,D是_____,G是_____,H是_____(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:__________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为_________。
(3)A中元素的原子结构示意图为________。
(4)F在溶液中的电离方程式为_________。
(5)上述反应中属于氧化还原反应的是_______(填写序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com