
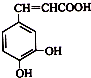
| A. | 该物质中苯环上一氯代物有2种 | |
| B. | 1 mol该物质可以与1.5 mol碳酸钠溶液反应生成1.5 mol CO2 | |
| C. | 既能发生取代反应,也能发生加成反应 | |
| D. | 所有碳原子不可能都在同一个平面上 |
分析 A.结构不对称,苯环上含3种H;
B.只有-COOH与碳酸钠反应生成二氧化碳;
C.含碳碳双键及苯环均可发生加成反应,含-OH、-COO均可发生取代反应;
D.苯环、碳碳双键均为平面结构,且直接相连.
解答 解:A.结构不对称,苯环上含3种H,则该物质中苯环上一氯代物有3种,故A错误;
B.只有-COOH与碳酸钠反应生成二氧化碳,酚-OH与碳酸钠反应生成酚钠和碳酸氢钠,则1 mol该物质可以与1.5 mol碳酸钠溶液反应生成0.5 mol CO2,故B错误;
C.含碳碳双键及苯环均可发生加成反应,含-OH、-COO均可发生取代反应,故C正确;
D.苯环、碳碳双键均为平面结构,且直接相连,则所有C原子可能共面,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力考查,注意烯烃、酚及羧酸的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 范德华力、范德华力 | B. | 范德华力、共价键 | ||
| C. | 共价键、范德华力 | D. | 共价键、共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
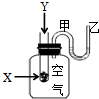 为了研究化学反应X+Y=Z的能量变化情况,某同学设计了如图所示装置.当向盛有X的试管中滴加试剂Y时,看到U型管中甲处液面下降乙处液面上升.试回答下列问题:
为了研究化学反应X+Y=Z的能量变化情况,某同学设计了如图所示装置.当向盛有X的试管中滴加试剂Y时,看到U型管中甲处液面下降乙处液面上升.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
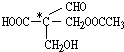 其中带*号的碳原子即是手性碳原子,现欲使该物质因不含手性碳原子而失去光学活性,下列反应中不可能实现的是( )
其中带*号的碳原子即是手性碳原子,现欲使该物质因不含手性碳原子而失去光学活性,下列反应中不可能实现的是( )| A. | 加成反应 | B. | 消去反应 | C. | 水解反应 | D. | 氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | C4H10O3 | B. | C5H12O4 | C. | C4H12O4 | D. | C5H12O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1NaHC2O4溶液(pH=5.5):c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| B. | 0.1mol•L-1NaHS溶液:c(OH-)+c(S2-)=c(H+)+c(H2S) | |
| C. | 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.1mol•L-1CH3COOH溶液和0.1mol•L-1CH3COONa溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
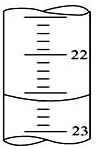 (I)、某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
(I)、某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com