
【题目】常温下,0.1 mol/L CH3COONa溶液pH=9,则下列说法正确的是
A. 加入少量NaOH固体后溶液pH小于9
B. 加水稀释,CH3COONa水解程度增大,c(OH-)增大
C. 该溶液水电离出的c(OH-)=10-9
D. CH3COOH在常温下Ka数值约为1×10-5
 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】下列化学反应的产物不止一种的是( )
A. CH3CH2CH2Br在碱性溶液中水解
B. 甲苯在催化剂作用下与Cl2发生苯环上的取代反应
C. ![]() 与NaOH的醇溶液共热反应
与NaOH的醇溶液共热反应
D. ![]() 在催化剂存在下与H2完全加成
在催化剂存在下与H2完全加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知KMnO4与浓盐酸在常温下反应能产生Cl2。若用下图所示的实验装置来制备纯净、干燥的氯气,并使它与金属反应。每个虚线框表示一个单元装置,其中错误的是
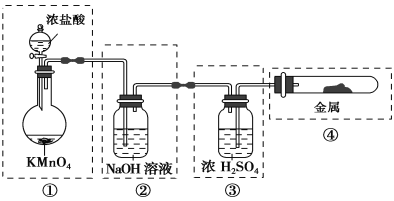
A. ①和②B. ②C. ②和③D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若m g Al在足量氯气中燃烧,生成固体的质量为(m+21.3)g,将m g Al投入总质量为95.2gNaOH水溶液中恰好完全反应。下列判断正确的是( )
A.m=2.7
B.Al与Cl2反应的产物溶于水,所得溶液中加入足量氨水,先出现沉淀,后又溶解
C.若在原NaOH溶液中通入足量Cl2,理论上可生成0.2molNaClO
D.Al与NaOH溶液反应后所得溶液中溶质的质量分数为16.4%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据物质的量的相关公式,完成下列问题。(注意书写单位)
(1)3.01×1023个NH3分子的物质的量__。
(2)0.5molH2SO4含有的氧原子的物质的量__。
(3)2.3gNO2的物质的量__。
(4)标况下,33.6LN2的物质的量___。
(5)0.5mol /LK2SO4溶液中,c(K+)=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中除含有Ca2+、Mg2+、SO42-等可溶性杂质外,还含有泥砂等不溶性杂质。
(1)检验溶液中含有SO42-的方法是_________________。
(2)将粗盐溶解过滤除去不溶性杂质后,在滤液中依次滴加过量NaOH溶液、BaCl2溶液和Na2CO3溶液,直至不再产生沉淀。这些操作的目的是_________________,滴加Na2CO3溶液时发生反应的化学方程式为________________。
(3)用提纯后的NaCl固体配制100mL l.0mol/LNaCl溶液,所用仪器除托盘天平、烧杯、玻璃棒、药匙外,还需要___________(填仪器名称)。转移溶液时没有洗涤烧杯会造成所配溶液浓度偏______(填“高”或“低”,下同),定容时仰视刻度线会造成所配溶液浓度偏____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨是我国丰产元素。科研专家经过长期勘测评审,于2016年元月确认江西省浮梁县存在着世界上最大的钨矿。从而进一步确立了江西省“世界钨都”的地位。自然界中钨有部分是以钨(+6价)酸盐的形式存在。黑钨矿的主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),含有SiO2、Al2O3等杂质。现用黑钨矿制备金属钨的流程图如图:
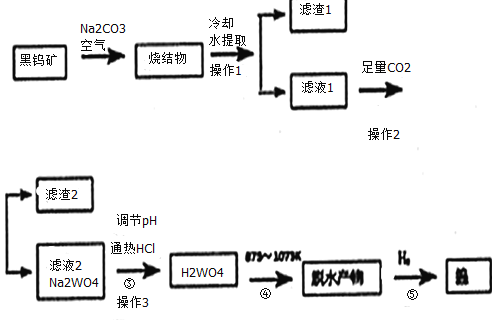
说明:a:反应①是在高温熔融下进行的,烧结物成分为:Fe2O3、Mn2O4、NaAlO2、Na2SiO3、Na2WO4
b:生成Fe2O3的反应为:4FeWO4+4Na2CO3+O2=4Na2WO4+4CO2+2Fe2O3
c:在pH值3.0~4.4的热溶液中,用盐酸沉淀出钨酸与杂质分离,灼烧后即为三氧化钨
回答下列问题:
(1)写出烧结物中生成Na2SiO3的化学反应方程式:__,生成Mn2O4与生成Fe2O3所发生的反应原理相同,请写出生成Mn3O4的化学反应方程式:___。
(2)操作3需要用到玻璃仪器的有:__。
(3)通入足量CO2时发生的离子反应方程式为:___、___。
(4)上述流程最后步骤中钨的制备属于工业冶炼金属的何种方法___。
(5)我国钨化学研究的奠基人顾翼东先生采用另外的反应制得了一种黄色的、非整比的钨的氧化物WO(3-x),这种蓝色氧化钨具有比表面大、易还原得优点。一般认为,蓝色氧化钨的颜色和非整比暗示了在化合物中存在正五价和正六价两种状态的钨,若x的值为0.1,则蓝色氧化钨中这两种价态的钨原子数之比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是

A. 洗气瓶中产生的沉淀是碳酸钡B. 洗气瓶中产生的沉淀是亚硫酸钡
C. 在Z导管出来的气体中没有二氧化碳D. 在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知O2F2可以发生反应:H2S+4O2F2 = SF6+2HF+4O2,下列说法正确的是( )
A.SF6是还原产物
B.O2F2是还原剂
C.若生成3.2g O2,则转移0.2 mol e
D.还原剂与氧化剂的物质的量之比为4:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com