
分析 NaOH中和的硫酸中n(H+)=2mol•L-1×0.025L=0.05mol,
与NH3反应的n(H+)=0.1L×0.5mol/L×2-0.05mol=0.05mol,
氨气和氢离子反应方程式为NH3+H+=NH4+,所以根据N原子守恒得n(NH4+)=0.05mol,
复盐中SO42-的质量分数为48%,则n(SO42-)=$\frac{10g×48%}{96g/mol}$=0.05mol,所以该复盐中n(NH4+):n(SO42-)=0.05:0.05=1:1,根据铵根离子和硫酸根离子关系计算x值;
根据硫酸根离子的物质的量计算复盐的物质的量,从而确定复盐相对分子质量,根据相对分子质量计算y值.
解答 解:NaOH中和的硫酸中n(H+)=2mol•L-1×0.025L=0.05mol,
与NH3反应的n(H+)=0.1L×0.5mol/L×2-0.05mol=0.05mol,
氨气和氢离子反应方程式为NH3+H+=NH4+,所以根据N原子守恒得n(NH4+)=0.05mol,
复盐中SO42-的质量分数为48%,则n(SO42-)=$\frac{10g×48%}{96g/mol}$=0.05mol,所以该复盐中n(NH4+):n(SO42-)=0.05:0.05=1:1,根据铵根离子和硫酸根离子关系得1+x=2x,x=1;
所以其化学式为CuSO4•(NH4)2SO4•yH2O,每个化学式中含有两个硫酸根离子,10g该复盐含有0.05mol硫酸根离子,所以复盐的物质的量为0.025mol,M[CuSO4•(NH4)2SO4•yH2O]=$\frac{10g}{0.025mol}$=400g•mol-1,
摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为400,所以18y+64+96×2+18×2=400,y=6.
故答案为:1;6.
点评 本题考查化学方程式有关计算,为高频考点,侧重考查学生分析计算能力,明确各个物理量之间的关系式是解本题关键,注意原子守恒的灵活运用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | C2H2、C2H4 | B. | C2H4、C3H6 | C. | C2H6、C3H8 | D. | CH4、C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
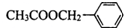 是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: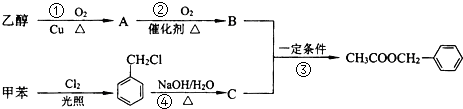
 +H2O$→_{△}^{氢氧化钠}$
+H2O$→_{△}^{氢氧化钠}$ +HCl;
+HCl;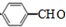 ;试写出遇FeCl3溶液显紫色,且符合以下条件的C的同分异构体的结构简式:
;试写出遇FeCl3溶液显紫色,且符合以下条件的C的同分异构体的结构简式: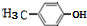
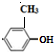 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCl | CO2 | 石灰水 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | Cl2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |
| ⑥ | NO2 | SO2 | BaCl2 |
| A. | ①②③④⑤ | B. | 只有②③④ | C. | 只有①③④ | D. | ①②③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入氢气即可发生加成反应 | |
| B. | 分子中含有3个C-C单键和三个C═C双键 | |
| C. | 分子中C、H元素的质量比为6:1 | |
| D. | 在空气中燃烧时产生浓烈的黑烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Fe3+、Br-、NO3- | B. | Na+、Ca2+、HCO3-、NO3- | ||
| C. | Al3+、NH4+、SO42-、Na+ | D. | Na+、K+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强 | B. | 不断鼓入空气 | C. | 加入FeS2 | D. | 升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
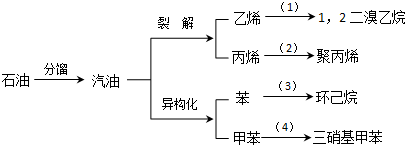
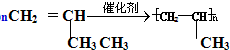 (加成聚合反应)
(加成聚合反应)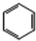 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$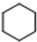 (加成反应)
(加成反应)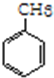 +3HO-NO2$→_{△}^{浓硫酸}$
+3HO-NO2$→_{△}^{浓硫酸}$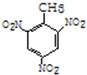 +3H2O(取代反应)
+3H2O(取代反应)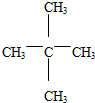 .
. .
.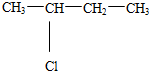 (不考虑顺反异构).
(不考虑顺反异构).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com