
【题目】a、b、c、d是四种短周期元素,a、b、c同周期,c、d同主族.a的原子结构示意图为 ![]() ,b与d形成的化合物的电子式为
,b与d形成的化合物的电子式为 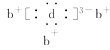 ,则下列叙述中正确的是( )
,则下列叙述中正确的是( )
A.原子序数:a>b>c
B.d单质最活泼
C.原子半径:a>c>d
D.最高价氧化物对应的水化物的酸性:d>a>c
【答案】C
【解析】解:a的原子结构示意图为 ![]() ,第一电子层容纳2个电子,故x=2,a的质子数为14,故a为Si元素;b与d形成的化合物的电子式为
,第一电子层容纳2个电子,故x=2,a的质子数为14,故a为Si元素;b与d形成的化合物的电子式为 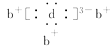 ,由电子式可知b原子核外有1个电子,且与Si同周期,应为Na元素,d原子核外有5个电子,且c、d同主族,可知c为P元素,d为N元素,
,由电子式可知b原子核外有1个电子,且与Si同周期,应为Na元素,d原子核外有5个电子,且c、d同主族,可知c为P元素,d为N元素,
A.a为Si,原子序数为14,b为Na,原子序数为11,c为P,原子序数为15,则原子序数c>a>b,故A错误;
B.d为N元素,单质含有N≡N键,键能较大,单质较稳定,故B错误;
C.同周期元素从左到右原子半径逐渐减小,同主族从上到下逐渐增大,为a>c>d,故C正确;
D.非金属性P>Si,磷酸酸性大于硅酸,故D错误.
故选C.
a的原子结构示意图为 ![]() ,第一电子层容纳2个电子,故x=2,a的质子数为14,故a为Si元素;b与d形成的化合物的电子式为
,第一电子层容纳2个电子,故x=2,a的质子数为14,故a为Si元素;b与d形成的化合物的电子式为 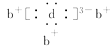 ,由电子式可知b原子核外有1个电子,且与Si同周期,应为Na元素,d原子核外有5个电子,且c、d同主族,可知c为P元素,d为N元素,以此解答该题.
,由电子式可知b原子核外有1个电子,且与Si同周期,应为Na元素,d原子核外有5个电子,且c、d同主族,可知c为P元素,d为N元素,以此解答该题.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】将0.2mol两种气态烃组成的混合气完全燃烧后得到6.72升二氧化碳(标准状况下)和7.2克水,下列关于该混合烃说法正确的是( )
A.一定有乙烯
B.一定有甲烷
C.一定没有甲烷
D.可能有乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、磷、硫元素的单质和化合物应用广泛.
(1)磷元素的原子结构示意图是 .
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2═6CaSiO3+P4O10 10C+P4O10═P4+10CO
每生成1mol P4时,就有mol电子发生转移.
(3)硫代硫酸钠(Na2S2O3)是常用的还原剂.在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量.发生的反应为:
C6H8O6+I2═C6H6O6+2H++2I﹣ 2S2O32﹣+I2═S4O62﹣+2I﹣
在一定体积的某维生素C溶液中加入a molL﹣1I2溶液V1mL,充分反应后,用Na2S2O3溶液滴定剩余的I2 , 消耗b molL﹣1Na2S2O3溶液V2mL.该溶液中维生素C的物质的量是mol.
(4)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3﹣+5SO32﹣+2H+═I2+5SO42﹣+H2O生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率.某同学设计实验如表所示:
0.01molL﹣1 | 0.01molL﹣1 | H2O的体积 | 实验 | 溶液出现蓝色时所需时间/s | |
实验1 | 5 | V1 | 35 | 25 | |
实验2 | 5 | 5 | 40 | 25 | |
实验3 | 5 | 5 | V2 | 0 |
该实验的目的是;表中V2=mL
(5)Ⅱ、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
铈(Ce)是地壳中含量最高的稀土元素.在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl36H2O和NH4Cl固体混合物的方法来制备.其中NH4Cl的作用是 .
(6)在某强酸性混合稀土溶液中加入H2O2 , 调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离.完成反应的离子方程式:Ce3++H2O2+H2O═Ce(OH)4↓+ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗定律成立的根本原因是在一定温度和压强下 ( )
A.气体体积的大小只随分子数量的多少而变化
B.不同气体分子的大小几乎相等
C.不同气体分子间的平均距离几乎相等
D.气体分子间的平均距离与分子本身的大小成正比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在呼吸面具和潜水艇中可用过氧化钠作供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。
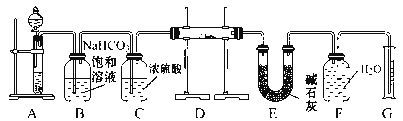
(1)A是制取CO2的装置。写出A中发生反应的化学方程式:____________________。
(2)B、C、E均为除杂装置(U型管中加固体干燥剂)除杂顺序如表:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | _________ |
C | 浓硫酸 | _________ |
E | 碱石灰 | _________ |
(3)写出B中发生反应的离子方程式:__________________________________。
(4)写出D中过氧化钠与二氧化碳反应的化学方程式:__________________。
(5)试管F中收集满气体后,证明试管中收集的气体是氧气的实验操作是:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Na2SO4、K2SO4、KCl的混和溶液中,如果c(Cl-)=0.1mol/L,c(Na+)=0.2mol/L,c(SO42-)=xmol/L,c(K+)=ymol/L,则x和y的关系是( )
A. x=0.5y B. 2x=0.1+y C. y=2(x-0.1) D. y=2x+0.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO![]() 、NO
、NO![]() 的相互分离。相应的实验过程可用下图表示:
的相互分离。相应的实验过程可用下图表示:
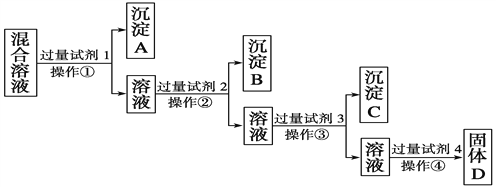
(1)写出上述实验过程中所用试剂的名称:试剂1为______________,试剂2为______________。
(2)控制试剂4的加入量的方法是__________________________。
(3)加入过量试剂3的目的是__________________________________。
(4)操作①的名称是________,在加入试剂4后,获得固体D的实验操作④是______________________(填操作名称)。
(5)写出加入试剂4后发生反应的化学方程式:
__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“化学,让生活更美好”,下列叙述不能直接体现这一主旨的是
A.风力发电,让能源更清洁B.合成光纤,让通讯更快捷
C.合成药物,让人类更健康D.环保涂料,让环境更宜居
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com