

���� ��I��������MnO2�õ����ӷ�����ԭ��Ӧ����Mn2O3������þʧ�������ɵ�þ���Ӻ��������������������þ������
��II����1���Ʊ�������Ҫ����װ�ú��ռ�װ�ã�β������װ�ã������Ʊ������õ�ԭ�ϵ�״̬�ͷ�Ӧ����ѡ����ʵķ���װ�ã������ж�������ֱ���ŷŵ������У��ܹ�������������Һ��Ӧ������������������Һ����������
��2������������ԭ��Ӧ���ɣ�������ǿ����ȡ��������������ѡ����ʵ��Լ���
��3���������������Ʒ�Ӧ�����ѹǿ��С��С��������ѹ���ձ��е���Һ�ᵹ�����Թܼף��������������Ʒ�Ӧ���������ɵĴ������ƾ���Ư���ԣ�
��4����Ӧ�л��ϼ۱仯��Ԫ��ΪMn��Cl��MnԪ����+4������Ϊ+6��ClԪ�ػ��ϼ���+5����Ϊ-1����ʧ������ȣ������ϼ�������ȣ����������������ص����ʵ���֮��Ϊ3��1���ٸ���ԭ���غ���ƽ�����Q=It��F=96500C/mol���������ת�����ʵ��������ݻ�ѧ����ʽ������ϵ����õ�����������ʵ������õ�������
��� �⣺��I��������MnO2�õ����ӷ�����ԭ��Ӧ����Mn2O3������þʧ�������ɵ�þ���Ӻ��������������������þ������Mg-2e-+2OH-=Mg��OH��2��
�ʴ�Ϊ����ԭ��Mg+2OH--2e-=Mg��OH��2��
��II����1���Ʊ�������Ҫ����װ�ú��ռ�װ�ã�β������װ�ã�ʵ�����ù������������Һ��Ũ���ᣬ�ڼ����������Ʊ�����������Ӧѡ����װ��A��
�����ж�������ֱ���ŷŵ������У��ܹ�������������Һ��Ӧ������������������Һ����������װ��ͼΪ��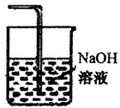 ��
��
�ʴ�Ϊ��A�� ��
��
��2���Ƚ�Cl-��Br-��ԭ��ǿ��������װ��C��ʢװ����Һ�廯�أ����廯�ƣ���Һ��������������ǿ���壬���ܹ��û��嵥�ʣ�
�ʴ�Ϊ���廯�أ����廯�ƣ���Һ��
��3�����������������Ʒ�Ӧ�����ѹǿ��С��С��������ѹ���ձ��е���Һ�ᵹ�����Թܼף������ȹر�ֹˮ��b��d���ٴ�ֹˮ�� c��˫�ֽ��գ����ȣ��Թܣ�ʹ�Թ��������ݳ���Cl2��NaOH��Һ�Ӵ���Һ�嵹����ʹ�ձ��е�Һ������Թܼף�Cl2��NaOH��Ӧ����NaCl�ʹ������ƣ���Һ���Լ��������Ҵ������ƾ���Ư���ԣ����Լ�����Һ����ɫ��
�ʴ�Ϊ��˫�ֽ��գ����ȣ��Թܼ�ʹ�Թ��������ݳ����ձ���������ð�������ˮ�������Թܼ��У�������Һ����ɫ��
��4�������̿����������KOH��KClO3�ڸ����·�Ӧ����������أ�K2MnO4����KCl����Ӧ�л��ϼ۱仯��Ԫ��ΪMn��Cl��MnԪ����+4������Ϊ+6��ClԪ�ػ��ϼ���+5����Ϊ-1�����ݵ�ʧ������ȣ������ϼ�������ȣ����������������ص����ʵ���֮��Ϊ3��1���ٸ���ԭ���غ���ƽ����ʽΪ3MnO2+6KOH+KClO3 $\frac{\underline{\;����\;}}{\;}$3K2MnO4+KCl+3H2O��
��֪����ܷ�Ӧ����ʽΪ��2K2MnO4+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2KMnO4+2KOH+H2���������K2MnO4��Һʱ��ά�ֵ���ǿ��Ϊ5.0A�����20min��ͨ������ΪQ=It=5.0A��20��60s=6000C��F=96500C/mol���������ʵ���=$\frac{6000C}{96500C/mol}$=0.062mol����ѧ����ʽ�����֪����ת��2mol����2molKMnO4�������ת��0.062mol����KMnO4���ʵ���ҲΪ0.062mol������=0.062mol��158g/mol��9.8g�������Ͽ�����KMnO4 ����Ϊ9.8g��
�ʴ�Ϊ��3��6��1��3��1��3��9.8��
���� ���⿼����ԭ���ԭ����Ӧ�á�������Ʊ������ʵļ��飬��Ϥ�����ı�ԭ���������ǽ���ؼ���������ѧ���ķ�������������������ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ȼ�����Һ�а�ɫ�������ɣ��ټ�ϡ���ᣬ��������ʧ����ԭ��Һ��һ����SO42- | |
| B�� | �����ռ���Һ����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ���������壬��ԭ��Һ��һ����NH4+ | |
| C�� | �������ᣬ�ų���ʹ�����ʯ��ˮ����ǵ���ɫ�����壬��ԭ��Һ��һ������CO32- | |
| D�� | ����AgNO3��Һ���а�ɫ�������ɣ���ԭ��Һ��һ������Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K | B�� | Ka | C�� | Kb | D�� | Kw |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2��NO��HCl��NH3��CO2 | B�� | O2��NO��NH3��HCl��SO2 | ||
| C�� | NO��O2��NH3��HCl��SO2 | D�� | HBr��Cl2��NH3��H2S��C2H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢܢޢ� | B�� | �ۢܢޢ� | C�� | �ܢݢޢ� | D�� | �ۢܢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �������������Ԫ�أ�����Ҫ��Ը����ߵ����ʳ�� | |
| B�� | �ý��ݹ����������Һ�Ĺ���������ˮ�������˼ӳɷ�Ӧ | |
| C�� | ʳƷ�������������ۡ��Ȼ��ơ�̿�۵ȣ�������ԭ���������������ʴ��ͬ | |
| D�� | ������������������Һ���ȣ�������ع��ͣ��ӹ����IJ��������ͣ�������ͣ����͡�ú�͡����͵ȣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ȼ�ϵ�� | B�� | п�̵�� | C�� | ���ӵ�� | D�� | Ǧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ������CO�����ܺ���CO2��O2 | B�� | ���ܺ���CO��һ������CO2��O2 | ||
| C�� | һ������C2O3�����ܺ���CO2��O2 | D�� | ����ֻ����C2O3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com