
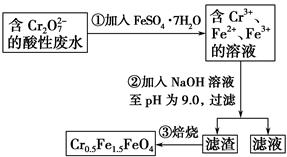
| A.操作①中反应的离子方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O |
| B.操作②所得的滤渣成分主要为Fe(OH)3、Fe(OH)2、Cr(OH)3 |
| C.磁性材料Cr0.5Fe1.5FeO4中,显+3价铁与显+2价铁的质量之比为2∶3 |
| D.若废水中杂质不与绿矾反应,将该1 L废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4,理论上需加入绿矾13.9 g |


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.将58.5 g NaCl溶于1 L水中可得1 mol·L-1的NaCl溶液 |
| B.将标准状况下22.4 L HCl溶于1 L水中可得1 mol·L-1盐酸 |
| C.将25.0 g胆矾溶于水后配成100 mL溶液所得溶液浓度为1 mol·L-1 |
| D.将78 g Na2O2溶于水,配成1 L溶液可得到浓度为1 mol·L-1溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 ,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3∶4,电子总数之比为3∶2。根据以上信息回答下列问题:
,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3∶4,电子总数之比为3∶2。根据以上信息回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 气体 | 烧瓶和气体的总质量(g) |
| A | 48.4082 |
| B | 48.4082 |
| C | 48.4082 |
| D | 48.4342 |
| E | 48.8762 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
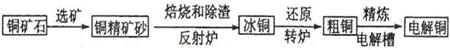
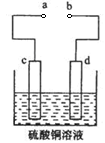
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.一维SiC纳米棒“比表面积”大,对微小粒子有较强的吸附能力 |
| B.上述反应中SiC既是氧化产物又是还原产物 |
| C.SiCl4是由极性键构成的非极性分子 |
| D.CCl4分子、SiCl4分子、SiC晶体中各原子都达到了8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.KI溶液, | B.淀粉溶液, | C.NaOH溶液, | D.氯水。发现溶液颜色按下面次序变化: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.16O与18O互为同位素; 、 、 、 、 、 、 互为同素异形体 互为同素异形体 |
| B.SiH4、PH3、HCl的稳定性逐渐增强 |
| C.氧化铁的化学式:FeO |
D.Ca2+的结构示意图为 ,NH4Cl的电子式为 ,NH4Cl的电子式为 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com