
【题目】在一定温度下,可逆反应A(g) + 3B(g)![]() 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A.容器内的压强不随时间变化
B.A、B、C的浓度不再变化
C.单位时间内生成n mol A,同时消耗2n mol C
D.A、B、C的分子数之比为1︰3︰2
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】图I是NO2(g)+CO(g)![]() CO2(g)+N0(g)反应过程中能量变化示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X增大的变化关系曲线如图II所示。下列有关说法正确的是
CO2(g)+N0(g)反应过程中能量变化示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X增大的变化关系曲线如图II所示。下列有关说法正确的是
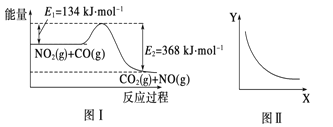
A. 该反应的焓变 △H=+234kJ/mol
B. 若X表示温度,则Y表示的可能是CO2的物质的量浓度
C. 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
D. 若X表示反应时间,则Y表示的可能是混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
A.CCl4中C原子sp3杂化,为正四面体形
B.BF3中B原子sp2杂化,为平面三角形
C.CS2中C原子sp1杂化,为直线形
D.H2S分子中,S为sp1杂化,为直线形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图所示装置对SO2的性质进行实验研究。
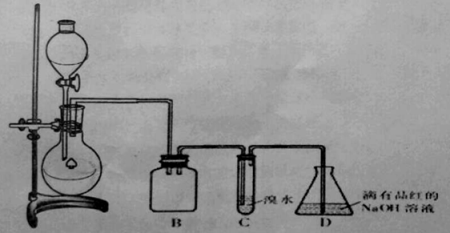
请回答下列问题:
(1)装置B的作用是 。
(2)装置C的目的是检验SO2 性。装置D中NaOH全部转化为NaHSO3的标志是 。
(3)向装置D所得NaHSO3溶液中加入漂白粉,有三种可能的情况:
I.HSO3-与ClO-刚好反应完 II.漂白粉不足 III.漂白粉过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定属于哪一种情况,请完成下表。
(已知酸性:H2SO4>H2CO3>HClO)
实验序号 | 实验操作 | 现象 | 可能的情况 |
① | 滴加少量淀粉-KI溶液,振荡 | III | |
② | 滴加少量溴水,振荡 | II | |
③ | 滴加少量酸性KMnO4溶液,振荡 | 溶液呈紫色 | |
④ | 加入几小块CaCO3固体 | 有气泡产生 |
(4)该小组同学认为,SO2通入含有BaCl2的双氧水中会出现白色沉淀,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示(某些条件和部分产物已略去)。下列说法错误的是
A.若戊为一种强碱且焰色反应为黄色,则反应①②可能都属于氧化还原反应
B.常温下,若丙为无色气体,戊为红棕色气体,则甲、乙是铜和稀硝酸
C.若甲为硫磺燃烧产物,丁为水,则戊可用于干燥甲
D.若甲为浓盐酸,乙为MnO2,则戊可能使品红褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组单质中,前者能将后者从化合物中置换出来的是
①Al、Fe ②C、Si ③Mg、C ④H2、Cu
A.只有①③ B.只有②④ C.①②③④ D.只有①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【离子反应】某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
阴离子 | Cl- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类与原溶液中种类相同。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1) 仅由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是___________(写离子符号)
(2) Ⅲ中加入少量盐酸生成无色气体的的离子方程式是______________________
(3) 将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为____________
(4) 甲同学最终确定原溶液中所含阳离子是___________,阴离子是______________(写
离子符号)
(5) 工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下是乙同学针对含
不同污染物的废水提出的处理措施和方法,其中正确的是__________________。
选项 | 污染物 | 处理措施 | 方法类别 |
A | 废酸 | 加生石灰中和 | 物理法 |
B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
D | 碱性的废水 | td style="width:106.85pt; border-top-style:solid; border-top-width:0.75pt; border-right-style:solid; border-right-width:0.75pt; border-left-style:solid; border-left-width:0.75pt; padding-right:5.03pt; padding-left:5.03pt; vertical-align:middle">化学法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a 的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子轨道示意图为 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为 ;分子中既含有极性共价键、又含有非极性共价键的化合物是 (填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是 ;酸根呈三角锥结构的酸是 。(填化学式)
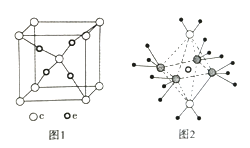
(4)e和c形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 。
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中,阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是 ,判断理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关,下列有关说法正确的是( )
A.消毒过程中细菌的蛋白质发生了盐析 B.用O3替代Cl2作饮用水消毒剂
C.鱼、虾等海鲜用福尔马林防腐保鲜 D.PH=5.6的雨水称为“酸雨”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com