
【题目】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。

⑴若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍;F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为_________________,反应④的化学方程式为________________________。
⑵若A为常见的金属单质,D、F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是______________________________________________。
⑶若A、D、F都是由短周期非金属元素形成的单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为__________________________________。
【答案】 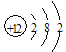 C+4HNO3(浓)
C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O 2Fe2++Cl2
CO2↑+4NO2↑+2H2O 2Fe2++Cl2![]() 2Fe3++2Cl- 2C+SiO2
2Fe3++2Cl- 2C+SiO2![]() 2CO↑+Si
2CO↑+Si
【解析】(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,则A原子序数是偶数,所含元素的原子最外层电子数D是A的2倍,A最外层电子数小于4且为偶数,D位于第二周期、A位于第三周期,则A是Mg、D是C元素;F的浓溶液与A、D反应都有红棕色气体生成,红棕色气体是NO2,则F是HNO3,C和HNO3浓溶液反应生成CO2、NO2和H2O,B能和Mg反应生成碳单质,则B是CO2,C是MgO,MgO和硝酸反应生成Mg(NO3)2和H2O,Mg和硝酸反应生成Mg(NO3)2,则E是Mg(NO3)2;
(2)若A是常见的金属的单质,D、F是气态单质,D和F反应生成B,B能够与金属A反应,则B为酸,为HCl,因此D为氢气,F为氯气,C为金属氯化物,能够与氯气反应,说明A具有变价,则A是Fe;因此C是FeCl2、E是FeCl3;
(3)A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则A为C,D为Si,F为O2,B为SiO2,反应①为C与二氧化硅的反应,C是CO,E为CO2。
(1)根据上述分析,A是Mg,A的原子结构示意图为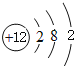 ,反应④为碳与浓硝酸的反应,反应的化学方程式为:C+4HNO3(浓)
,反应④为碳与浓硝酸的反应,反应的化学方程式为:C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O,故答案为:
CO2↑+4NO2↑+2H2O,故答案为: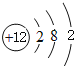 ;C+4HNO3(浓)
;C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2)根据上述分析,反应②为氯气氧化氯化亚铁的反应,反应的离子方程式是:2Fe2++Cl2═2Fe3++2Cl-,故答案为:2Fe2++Cl2═2Fe3++2Cl-;
(3)根据上述分析,A为C,D为Si,F为O2,B为SiO2,C是CO,E为CO2,反应①为C与二氧化硅的反应,反应方程式为:2C+SiO2![]() Si+2CO↑,故答案为:2C+SiO2
Si+2CO↑,故答案为:2C+SiO2![]() Si+2CO。
Si+2CO。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】认识反应条件对化学反应的影响,对学好化学具有重要意义。下列说法中正确的是
A.硫在空气中或纯氧中燃烧,主要产物都是SO2
B.钠在空气中缓慢氧化或在空气中燃烧,产物都是Na2O2
C.铁片在常温下与稀硫酸或浓硫酸反应,都生成FeSO4
D.镁在空气中或纯氧中燃烧,产物都只有MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石油裂解气为原料,通过一系列化学反应可得到重要的化工产品增塑剂G。

请完成下列各题:
(1)写出反应类型:反应①__________________,反应④____________________。
(2)写出反应条件:反应③__________________。
(3)反应②③的目的是:________________________________________________。
(4)写出反应⑤的化学方程式:__________________________________________。
(5)B被氧化成C的过程中会有中间产物生成,检验该物质存在的试剂是_______________________________________________。
(6)1,3-丁二烯与一定量的H2在一定条件下的加成产物中存在顺反异构,写出顺式产物结构简式_________________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于 ,下列结论正确的是( )
,下列结论正确的是( )
A. 该有机物分子式为C13H16 B. 该有机物属于苯的同系物
C. 该有机物分子至少有4个碳原子共直线 D. 该有机物分子最多有13个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某化学课外小组用如右图一装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。

(1)观察到A中的现象是_________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡, 写出有关反应的化学方程式 _________________。
(3)C中盛放CCl4的作用是_____________________________________________。
(4)若证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是 ______________________________。
II.实验室制备硝基苯的主要步骤如下:①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中;②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;③在50~60℃下发生反应,直至反应结束;④除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤;⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净的硝基苯。 请填写下列空白:
(1)配制一定比例浓硫酸和浓硝酸混合酸时,正确操作是___________________________。
(2)步骤③中,为了使反应在50~60℃下进行,常用的方法是_________________________。
(3)步骤④中粗产品用5%NaOH溶液洗涤的目的是 _________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用石墨烯和具有粘弹性的聚硅树脂(俗称橡皮泥)制备出一种具有极高 灵敏度的电力学传感材料,能够检测轻微的变形和冲击,其灵敏程度甚至能探测到蜘蛛的运动。该材料可用于制作检测人体脉搏、血压的传感器等。实验室模拟工业合成方法,制备聚硅树脂的中间体氯甲基三乙氧基硅烷ClCH2Si(OEt)3 。量取20mL甲基三氯硅烷(CH3SiCl3)注入三口烧瓶中,开启电磁搅拌加热器升温至66℃,从a中加入浓盐酸,加热A一段时间,待温度升至110℃,停止加热,在三口烧瓶中加入30mL无水乙醇(EtOH),迅速反应生成氯甲基三乙氧基硅烷ClCH2Si(OEt)3,待温度降至室温后,将三口烧瓶中液体转移到蒸馏烧瓶中蒸馏,收集得到174.5℃馏分12mL。
物质 | C2H5OH | CH3SiCl3 | ClCH2SiCl3 | ClCH2Si(OEt)3 |
相对分子质量 | 46 | 149.5 | 184 | 212.5 |
熔点/℃ | -114.1 | -77.8 | — | — |
沸点/℃ | 78.3 | 66.4 | 116.5 | 174 |
密度/g·mL | 0.79 | 1.30 | 1.47 | 1.02 |
已知:甲基三氯硅烷为无色液体,具有刺鼻恶臭,易潮解;氯甲基三乙氧基硅烷易水解,能与碱金属氢氧化物生成碱金属硅醇盐。

(1)连接好装置后,检验装置气密性的操作是:_________________________________;
(2)A装置中发生反应的离子方程式是:_______________________________________;
装置C的作用是:_____________________ ;E中所装液体是:______________;
(3)装置D中发生反应的化学方程式为:① CH3SiCl3 + Cl2 → ClCH2SiCl3 + HCl
②__________________________________________________________________ ;
球形冷凝管的作用是:________________________;
(4)有同学发现该装置有一处不足可能会导致实验失败,应该__________________________________________________;
(5) 该方法制备氯甲基三乙氧基硅烷的产率是:_______________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的以离子形式存在的碘元素。下图是实验室从海藻中提取碘的流程的一部分。

下列判断正确的是
A. 步骤①、③的操作分别是过滤、萃取分液
B. 步骤②的反应是非氧化还原反应
C. 步骤③中加入的有机溶剂可以是己烯或四氯化碳
D. 步骤④的操作是过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com