
 (1)用作橡胶工业的硫化剂S2Cl2的分子结构中每个原子均满足8电子稳定结构,①试写出S2Cl2的电子式
(1)用作橡胶工业的硫化剂S2Cl2的分子结构中每个原子均满足8电子稳定结构,①试写出S2Cl2的电子式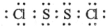 .
.分析 (1)①S2Cl2分子结构与H2O2相似,S2Cl2分子中氯原子与硫原子之间形成1对共用电子对,硫原子与硫原子之间形成1对共用电子对;
②依据现象分析判断产物为硫单质、二氧化硫和氯化氢,根据氧化还原反应的元素化合价变化守恒和原子守恒写出;
(2)①物质的量浓度c=$\frac{n}{V}$;
②在Ag+的作用下,过二硫酸盐将Mn2+氧化为MnO4-,同时自身被还原为硫酸根离子;
(3)Na2S2O4暴露于空气中易被氧气氧化,则氧化剂为氧气,还原剂为Na2S2O4,根据得失电子守恒计算反应后产物;
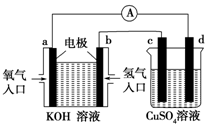
(4)左边装置是燃料电池,通入氢气的电极是负极、通入氧气的电极是正极,右边装置在电解池,左边Cu是阴极、右边Cu是阳极,阳极上Cu失电子发生氧化反应;通入氧气的电极上氧气得电子和水反应生成氢氧根离子.
解答 解:(1)①S2Cl2分子结构与H2O2相似,S2Cl2分子中氯原子与硫原子之间形成1对共用电子对,硫原子与硫原子之间形成1对共用电子对,S2Cl2电子式为 ,
,
故答案为: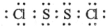 ;
;
②S2Cl2与水反应,有无色刺激性气味气体产生,并有黄色沉淀生成,无色刺激性气味气体除氯化氢外,依据氧化还原反应的元素化合价变化守恒推断,化合价降低的生成黄色沉淀为单质硫,化合价升高的生成二氧化硫气体,依据原子守恒、电子守恒写出化学方程式为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑,
故答案为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.
(2)①若硫酸铵溶液的浓度为250g/L=$\frac{\frac{250g}{132g/mol}}{1L}$=1.89 mol/L,
故答案为:1.89;
②在Ag+的作用下,过二硫酸盐将Mn2+氧化为MnO4-,同时自身被还原为硫酸根离子,离子方程式为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+10H+,
故答案为:2Mn2++5S2O82-+8H2O$\frac{\underline{\;Ag+\;}}{\;}$2MnO4-+10SO42-+10H+;
(3)Na2S2O4暴露于空气中易被氧气氧化,则氧化剂为氧气,还原剂为Na2S2O4,又氧化剂和还原剂的物质的量之比为l:1,设Na2S2O4被氧化后硫的化合价为+x价,则根据得失电子守恒,1×4=1×2×(x-3),解得x=5,又有水蒸气参与反应,所以产物为NaHSO4 和NaHSO3,
故答案为:NaHSO4 和NaHSO3;
(4)左边装置是燃料电池,通入氢气的电极是负极、通入氧气的电极是正极,右边装置在电解池,左边Cu是阴极、右边Cu是阳极,阳极上Cu失电子发生氧化反应,电极反应式为Cu-2e-=Cu2+,通入氧气的电极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,
故答案为:Cu-2e-=Cu2+;O2+2H2O+4e-=4OH-.
点评 本题考查较综合,涉及原电池原理、电子式书写、氧化还原反应及其电荷守恒等知识点,为高频考点,难点是电极反应式的书写,要结合电解质溶液酸碱性书写;注意氧化还原反应电子转移的计算,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | c(N2)=2.25 mol/L | B. | c(NH3)=1.9 mol/L | C. | c(H2)=0.3 mol/L | D. | c(N2)=1.3mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
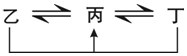 有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、并能使红色湿润石蕊试纸变蓝,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.下图中均含D或F元素的物质均会有图示转化关系:
有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、并能使红色湿润石蕊试纸变蓝,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.下图中均含D或F元素的物质均会有图示转化关系: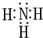 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的化学性质比乙烷活泼 | B. | 乙烯的比例模型可表示为  | ||
| C. | 可作香蕉等水果的催熟剂 | D. | 燃烧时火焰明亮,同时产生黑烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol HNO3见光分解,转移的电子数为4NA | |
| B. | 25℃时,1LpH=1的H2SO4溶液中含有的H+数为0.1NA | |
| C. | 28 g乙烯与丙烯的混合物中含有的共用电子对数为6NA | |
| D. | 将0.5molNH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+的数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为检验SO42-需要滴加稀硝酸酸化的BaCl2溶液并观察是否有白色沉淀生成 | |
| B. | 把光洁无锈的铁丝放在煤气灯外焰灼烧至与原来的火焰颜色相同时,蘸取K2CO3溶液并灼烧,透过蓝色钴玻璃可观察到火焰为淡紫色 | |
| C. | 向盛有足量苯酚溶液的试管中滴加少量稀溴水,可观察到白色沉淀生成 | |
| D. | 实验室制备乙炔时,常用NaOH溶液除去产生的H2S、PH3等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷是正四面体结构,性质活泼,常温下能与强酸、强碱发生剧烈反应 | |
| B. | 乙烯是通过石油裂解得到的,属于不饱和烃 | |
| C. | 苯与氢气、液溴、浓硝酸的反应类型相同 | |
| D. | 乙酸又名醋酸,其官能团是醚基,可以与乙醇发生反应生成乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| B. | 乙醇发生催化氧化反应,产物可用新制的Cu(OH)2悬浊液检验 | |
| C. | 加入浓CuSO4溶液能使蛋白质溶液发生盐析现象 | |
| D. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |||
| Y | Z |
| A. | 氢化物沸点:W<Z | B. | 氧化物对应水化物的酸性:Y>W | ||
| C. | 化合物熔点:Y2X3<YZ3 | D. | 简单离子的半径:Y<X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com