
| A. | Na与H2O的反应是熵增的放热反应,该反应能自发进行 | |
| B. | 饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 | |
| C. | FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 | |
| D. | Mg(OH)2固体在溶液存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
分析 A.该反应为固体与液态反应生成气体,该反应为熵增反应,反应放出大量的热,结合△G=△H-T△S<0,反应自发进行;
B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,前者为盐析,后者为蛋白质变性;
C.FeCl3和MnO2对H2O2分解催化效果不相同;
D.NH4Cl溶液中铵根离子水解呈酸性,消耗Mg(OH)2(s)溶解平衡中的氢氧根离子,平衡右移.
解答 解:A.Na与水反应为固体与液态反应生成气体,该反应为熵增反应,即△S>O,反应中钠熔化为小球,说明反应放出大量的热,即△H<0,则△G=△H-T△S<0,故该反应自发进行,故A正确;
B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,饱和Na2SO4溶液降低蛋白质溶解度,为盐析现象,为可逆过程,再加入水可以溶解,硝酸具有强氧化性,使蛋白质变性,过程不可能,二者原理不同,故B正确;
C.FeCl3和MnO2对H2O2分解催化效果不相同,同等条件下H2O2分解速率的改变不相同,故C错误;
D.NH4Cl溶液中铵根离子水解呈酸性,消耗Mg(OH)2(s)溶解平衡中的氢氧根离子,使Mg(OH)2(s)?Mg2+(aq)+2OH-(aq)平衡右移,故Mg(OH)2可溶于NH4Cl溶液,故D正确,
故选:C.
点评 本题侧重对化学反应原理考查,涉及反应自发性判断、蛋白质的性质、反应速率影响因素、沉淀溶解平衡等,注意B选项中蛋白质变性的一些方法,难度不大.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 滴定前,盐酸和醋酸溶液中:c(Cl?)<c(CH3COO-) | |
| B. | 分别加入10.00 mL NaOH溶液时,测得醋酸反应后所得溶液pH=6,则溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$>1 | |
| C. | 当两种溶液的pH均等于7时,两种酸所消耗NaOH溶液体积不相等,醋酸消耗的NaOH溶液体积多 | |
| D. | 加入20.00 mL NaOH溶液时,所得两种溶液中:c(Cl?)<c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
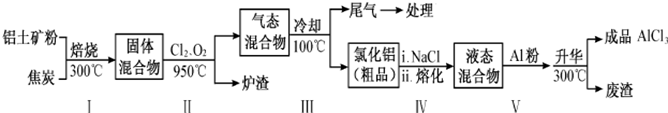
| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
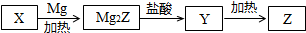
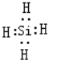 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 电解饱和食盐水可制得金属钠 | B. | 海带提碘只涉及物理变化 | ||
| C. | 海水提溴涉及到氧化还原反应 | D. | 海水提镁涉及到复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
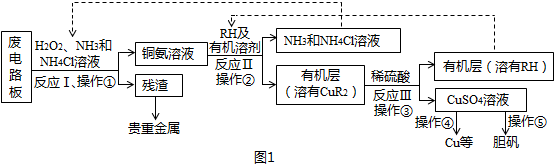
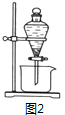
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- | |
| D. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1803 年道尔顿提出的“元素的原子以其原子质量为特征” | |
| B. | 1808 年盖•吕萨克提出的“同温同压下,相同体积的不同气体含有相同数目的原子” | |
| C. | 1811 年贝来里乌斯提出的“不同原子显不同电性,因而产生吸引力形成化合物“ | |
| D. | 1887 年阿伦尼乌斯提出的“电解质在溶液中会自发离解成带电的粒子” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、OH-、Ba2+、NO3- | B. | Al3+、AlO2-、HCO3-、Na+ | ||
| C. | Na+、Fe3+、SO42-、I- | D. | Fe3+、SCN-、Na+、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com