��ֹ������������Ⱦ�ǵ�ǰ������������Ҫ�о�����֮һ��
��1�����ʳ��İ�����ˮ��������������ɵõ���Ũ�Ȱ�����ˮ�����������������£�
��Ũ�Ȱ�����ˮ
��HNO
3��ˮ
����ˮ
����I��������ϸ�������£�O
2��NH
4+����ΪNO
3-������II������״���NO
3-�ͼ״���Ӧת��CO
2��N
2����д������I�������ӷ���ʽ��
��
��2��Hg��ˮ����Ⱦ���ؽ���Ԫ��֮һ��ˮ��Һ�ж��۹�����Ҫ������̬��Cl
-��OH
-��Ũ�ȹ�ϵ��ͼ1��ʾ[ͼ�е����ʻ�����ֻ��Hg��OH��
2�����pC1=-1gc��C1
-��]
������˵������ȷ����
��
A��������Hg
2+ˮ�⣬����Hg��NO
3��
2��ҺʱӦ��Hg��NO
3��
2��������Ũ�������ϡ�ͣ�
B����c��C1
-��=10
-1mol?L
-ʱ����Ԫ��һ��ȫ����HgCl
42-��ʽ����
C��HgCl
2��һ��������ʣ�����뷽��ʽ�ǣ�HgCl
2=HgCl
++C1
-D������ҺpH������4��pCl��2�ı���6ʱ����ʹHgCl
2ת��ΪHg��OH��
2��HgCl
2�ֳơ����������۵�549K���������������侧����
��������ͣ���
��3������β���dz��п�����Ⱦ��һ����Ҫ���أ��������·�Ӧ��������β����
2NO��g��+2CO��g��
2CO
2��g��+N
2��g��
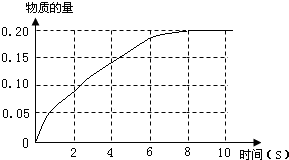
��ij�¶�T
1���£�2L�ܱ������г���NO��CO��0.4mol����ò�ͬʱ���NO��CO���ʵ������±���
| ʱ�䣨s�� | 0 | 2 | 4 | 6 | 8 | 10 |
| n��NO����mol�� | 0.4 | 0.32 | 0.26 | 0.22 | 0.20 | 0.20 |
�ٸ����ϱ������ݣ���ͼ2�л���CO
2�����ʵ�����ʱ��Ĺ�ϵ���ߣ�
��������Ӧ�ﵽƽ���������NO��CO��CO
2��0.2mol
��N
2
molʱ��ƽ�ⲻ�ƶ���
�������������¸÷�Ӧ�ܹ��Է����У�������¶ȴ�T
1�����ߵ�T
2�棬ƽ�ⳣ��K��
����д���������С���������䡱����
��һ��CO�����ǵĴ������ɲⶨ����β���Ƿ�����ŷű����÷����ǵĹ���ԭ������ȼ�ϵ�أ����еĹ���������Y
2O
3-Na
2O��O
2-���������������ƶ��������ķ�ӦʽΪ
��



 ��
��

 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
 ��������֮���ת������ѧϰԪ�ػ�����֪ʶ�Ļ�����
��������֮���ת������ѧϰԪ�ػ�����֪ʶ�Ļ�����