
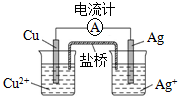
���� ��1�����ڷ����ڿ����е�����Ʒ����������ڣ������������Ϳ����е������ⷢ���˷�Ӧ���ɺ�ɫ��Ag2S��
��2��n��AgNO3��=0.05L��0.018mol/L=0.0009mol��n��HCl��=0.05L��0.020mol/L=0.001mol����������HCl������ӦAgNO3+HCl=AgCl��+HNO3�����ݷ���ʽ֪��HClʣ�࣬����������Һ��c��Cl-������Һ��c��Ag+��=$\frac{{K}_{sp}}{c��C{l}^{-}��}$��ʵ���������Ӳ��μӷ�Ӧ���ó���Һ��c��H+�����ٸ�����Һ��pH=-lgc��H+�����㣻
��3������ɫ������NO2���÷�Ӧ��AgԪ�ػ��ϼ���+1�۱�Ϊ0�ۡ�NԪ�ػ��ϼ���+5�۱�Ϊ+4�ۣ�����������ԭ��Ӧ֪������Ԫ��ʧ���ӻ��ϼ����ߣ�ֻ����OԪ��ʧ��������O2�����ݷ�Ӧ������P��Ӧ������д����ʽ��
��4����ԭ����У�Cu�Ļ�Դ���Ag��Cu��ʧ���ӷ���������Ӧ������Cu�Ǹ�����Ag�������������������ӵõ��ӷ�����ԭ��Ӧ��
��� �⣺��1�����ڷ����ڿ����е�����Ʒ����������ڣ������������Ϳ����е������ⷢ���˷�Ӧ���ɺ�ɫ��Ag2S��
�ʴ�Ϊ��Ag���������H2S��Ӧ���ɺ�ɫ��Ag2S��
��2��n��AgNO3��=0.05L��0.018mol/L=0.0009mol��n��HCl��=0.05L��0.020mol/L=0.001mol����������HCl������ӦAgNO3+HCl=AgCl��+HNO3�����ݷ���ʽ֪��HClʣ�࣬�����Һ��c��Cl-��=$\frac{��0.001-0.0009��mol}{0.05L+0.05L}$=10-3 mol/L����Һ��c��Ag+��=$\frac{{K}_{sp}}{c��C{l}^{-}��}$=$\frac{1.8��1{0}^{-10}}{1{0}^{-3}}$mol/L=1.8��10-7mol/L��ʵ���������Ӳ��μӷ�Ӧ������Һ��c��H+��=$\frac{0.001mol}{0.05L+0.05L}$=0.01mol/L����Һ��pH=-lgc��H+��=-lg0.01=2��
�ʴ�Ϊ��1.8��10-7��2��
��3������ɫ������NO2���÷�Ӧ��AgԪ�ػ��ϼ���+1�۱�Ϊ0�ۡ�NԪ�ػ��ϼ���+5�۱�Ϊ+4�ۣ�����������ԭ��Ӧ֪������Ԫ��ʧ���ӻ��ϼ����ߣ�ֻ����OԪ��ʧ��������O2�����ݷ�Ӧ������P��Ӧ������д����ʽΪ2AgNO3$\frac{\underline{\;����\;}}{\;}$2Ag+2NO2��+O2����
�ʴ�Ϊ��2AgNO3$\frac{\underline{\;����\;}}{\;}$2Ag+2NO2��+O2����
��4����ԭ����У�Cu�Ļ�Դ���Ag��Cu��ʧ���ӷ���������Ӧ������Cu�Ǹ�����Ag�������������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪAg++e-=Ag��
�ʴ�Ϊ��Ag++e-=Ag��
���� ���⿼��ԭ���ԭ����������ԭ��Ӧ��pH���㡢�ܶȻ�������֪ʶ�㣬�ۺ��Խ�ǿ����ȷ�������жϼ��䷢���ķ�Ӧ���ܶȻ��������塢������ԭ��Ӧ���ʵ�֪ʶ�㼴�ɽ��ע�⣨2����Ҫ���й������㣬Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NA��Fe��OH��3�������ӵ�����Ϊ107 g | |
| B�� | 8.0 g Cu2S��CuO�Ļ�����к���ͭԭ����Ϊ0.1NA | |
| C�� | ��״���£�2.24 L Cl2����ˮ�дﵽ���ͣ��ɵõ�HClO���ӵ���Ŀ��0.1NA | |
| D�� | 1 mol Na2O2�����к���������Ϊ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ɫʯ����ֽ | B�� | ��������Һ | ||
| C�� | �������ɫ���� | D�� | ʪ��ĵ⻯�ص�����ֽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij�¶�ʱ����2L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯������ͼ��ʾ��
ij�¶�ʱ����2L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
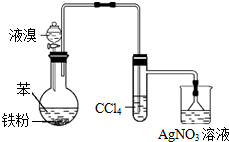
| A�� | ��װ����CCl4�������dz�ȥ����HBr�л��е�Br2���� | |
| B�� | ����Һ���ΪŨ��ˮ���÷�ӦҲ�ܽ��� | |
| C�� | ͨ��AgNO3��Һ���е���ɫ����������˵���ɱ����屽�ķ�Ӧ��ȡ����Ӧ | |
| D�� | ��װ���������ܵ������ǵ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ��ѧ������1ͼ��ʾװ��֤����ͱ��ķ�Ӧ��ȡ����Ӧ�����Ǽӳɷ�Ӧ����Ҫʵ�鲽�����£�
��ѧ������1ͼ��ʾװ��֤����ͱ��ķ�Ӧ��ȡ����Ӧ�����Ǽӳɷ�Ӧ����Ҫʵ�鲽�����£� �����13��ԭ�ӹ�ƽ�森
�����13��ԭ�ӹ�ƽ�森�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
| ���������mL�� | 50 | 120 | 232 | 290 | 310 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��H2O��Ӧ��Na+2H2O�TNa++2OH-+H2 | |
| B�� | Na�����ᷴӦ��2Na+2H+�T2Na++H2�� | |
| C�� | ��Ͷ��CuSO4��Һ�У�Cu2++2Na�TCu+2Na+ | |
| D�� | Na��O2��Ӧ��4Na+O2�T4Na++2O2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com