
下列叙述中,能证明某物质是强电解质或弱电解质的是( )
|
| A. | 某物质熔化时不导电,则该物质为弱电解质 |
|
| B. | 某物质不是离子化合物,而是极性共价化合物,则该物质为弱电解质 |
|
| C. | 某一元酸2 mol与足量Zn完全反应生成1 molH2,则该酸为强酸 |
|
| D. | 溶液中已电离的离子和未电离的分子共存,则该物质为弱电解质 |
考点:
弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐,以此解答.
解答:
解:A.熔化时不导电,说明没有自由移动的离子,但不是弱电解质的特征,如蔗糖是非电解质,HCl为强电解质,熔化时不导电,故A错误;
B.电解质的强弱是根据其电离程度划分的,与是离子化合物还是共价化合物无关,如HCl为极性化合物,但为强电解质,故B错误;
C.无论强酸还是弱酸,如完全反应,则一元酸2 mol与足量Zn完全反应生成1 molH2,故C错误;
D.溶液中溶质电离出的离子与未电离的分子共同存在,说明该溶质只有部分电离,所以为弱电解质,故D正确.
故选D.
点评:
本题考查了弱电解质的判断,根据电解质的电离程度来判断,易错选项是C,注意电解质的强弱与溶液导电能力无关,强电解质溶液的导电能力不一定强,导电能力强的溶液不一定是强电解质溶液,为易错点.


科目:高中化学 来源: 题型:
X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17.
请填空:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”): ,理由是
(2)Y是 ,Z是 ,W是 ;
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1.写出该化合物的名称及化学式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体.铜液吸收CO的反应是放热反应,其化学方程式为:Cu(NH3)2Ac+CO+NH3⇌[Cu(NH3)3CO]Ac,若要提高上述反应的正反应速率,可采取的措施是
①增加NH3的浓度 ②降温 ③减压 ④及时移走产物()
A. ① B. ②③ C. ③④ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列指定反应的离子方程式正确的是()
A. Cu溶于稀硝酸:Cu+2H++NO3﹣→Cu2++NO2↑+H2O
B. 在复盐NH4Fe(SO4)2溶液中逐滴加入一定量的Ba(OH)2溶液:2Fe3++3SO42﹣+3Ba2++6OH﹣→3BaSO4↓+2Fe(OH)3↓
C. 向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸:2OH﹣+CO32﹣+4H+→CO2↑+3H2O
D. 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2﹣+2H2O=Al(OH)3↓+HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
1,6﹣已二酸(G)是合成尼龙的主要原料之一,可用含六个碳原子的有机化合物氧化制备.如图为A通过氧化反应制备G的反应过程(可能的反应中间物质为B、C、D、E和F):
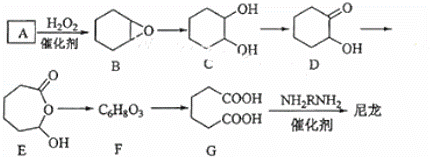
回答下列问题:
(1)化合物A中含碳87.8%,其余为氢,A的化学名称为 .
(2)B到C的反应类型为 .
(3)F的结构简式为 .
(4)在上述中间物质中,核磁共振氢谱出峰最多的是DE,最少的是F.(填化合物代号)
(5)由G合成尼龙的化学方程式为 .
(6)由A通过两步反应制备1,3﹣环已二烯的合成路 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )
|
| A. |
FeCl3+3KSCN⇌Fe(SCN)3+KCl(忽略液体体积变化) |
|
| B. |
2NO+O2⇌2NO2△H<0 |
|
| C. |
NO(g)+CO(g)⇌ |
|
| D. |
A2(g)+3B2(g)⇌2AB3(g)△H=﹣373.4KJ•mol﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应:N2(g)+3H2(g)⇌2NH3(g)△H<0.在等容条件下进行.体系中各物质浓度随时间变化的曲线如图1所示,回答问题:
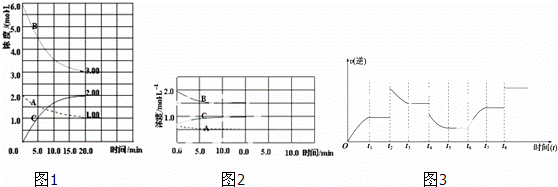
(1)图1中B为 (填“N2”、“H2”或“NH3”)计算反应从开始→达平衡时H2的反应速率v(H2)=
(2)图1是在某温度下反应达到平衡,将容器的体积扩大一倍,假定10min后达到新的平衡,请在图2中用曲线表示体系中各物质的浓度随时间变化的趋势(不需计算新平衡时的具体浓度,只要新平衡时浓度处于一个合理范围内即可.曲线上必须标出N2、H2、NH3).
(3)若该反应的逆反应速率与时间的关系如图3所示:反应在t1、t3、t5、t7时都达到了平衡,而t2、t4、
t6、t8时都改变了条件,试判断改变的条件是(填“升温”、“降压”…等);t2时 ;t6时 ;t4时,平衡向 (填“正”或“逆”)反应方向移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,列各项正确的是( )
-A. mol•L﹣1 NaCl溶液含有NA个Na+
-B.-标准状况下,分子数为NA的CO、N2的混合气体体积约为22.4 L,质量为28 g
-C.-标准状况下,22.4 L空气含有NA个单质分子
-D.2.4 L O2所含的原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:正确的操作顺序是( )
①加入稍过量的Na2CO3溶液;
②加入稍过量的NaOH溶液;
③加入稍过量的BaCl2溶液;
④滴入稀盐酸至无气泡产生;
⑤过滤.
|
| A. | ③②①⑤④ | B. | ①②③⑤④ | C. | ②③①④⑤ | D. | ③⑤②①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com