
某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72—转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,完成以下实验设计表(表中不要留空格)。

测得实验①和②溶液中的Cr2O72—浓度随时间变化关系如图所示。

(2)上述反应后草酸被氧化为______________(填化学式)。
(3)实验①和②的结果表明________;实验①中0~t1时间段反应速率v(Cr3+)=________mol·L-1·min-1(用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用;
假设二:________;
假设三: ________;
……
(5)请你设计实验验证上述假设一,完成下表中内容。[除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。溶液中Cr2O72—的浓度可用仪器测定]
实验方案 (不要求写具体操作过程) | 预期实验结果和结论 |
|
|
(1)

(2)CO2
(3)溶液pH对该反应的速率有影响 2(c0-c1)/t1
(4)Al3+起催化作用 SO42—起催化作用
(5)
实验方案 (不要求写具体操作过程) | 预期实验结果和结论 |
用等物质的量K2SO4·Al2(SO4)3·24H2O代替实验①中的铁明矾,控制其他反应条件与实验①相同,进行对比实验 | 反应进行相同时间后,若溶液中c(Cr2O72—)大于实验①中的c(Cr2O72—),则假设一成立;若两溶液中的c(Cr2O72—)相同,则假设一不成立 |
(本题属于开放性试题,合理答案均可)
【解析】首先看清实验目的,确定条件改变的唯一变量,再根据图给信息进行综合分析;对于实验方案的设计也主要考虑变量的控制。
(1)要保证其他量不变,草酸用量为唯一变量,必须保证溶液的体积为100 mL,所以加入草酸和水的体积之和应为40 mL,两者的具体体积没有要求,只需与②中数据不同即可。(2)此反应中铬的化合价由+6价变为+3价,化合价降低,所以碳的化合价应升高,草酸中碳的化合价为+3价,反应后只能变为+4价,即生成CO2。(3)通过图像可以明显看到,实验①的反应速率比实验②的快,故pH越小,反应速率越快,说明溶液pH对该反应的速率有影响;在0~t1时间段,Cr2O72—的浓度改变了(c0-c1)mol·L-1,其反应速率为(c0-c1)/t1 mol·L-1·min-1,所以v(Cr3+)=2(c0-c1)/t1 mol·L-1·min-1。(4)铁明矾中除结晶水外,共有三种离子,均可能起催化作用,除Fe2+外,还有Al3+和SO42—。(5)要想验证假设一正确,必须确定Al3+和SO42—不起催化作用,所以可选择K2SO4·Al2(SO4)3·24H2O,为了确保Al3+和SO42—的浓度与原来的相同,所以取和铁明矾相同物质的量的K2SO4·Al2(SO4)3·24H2O。
点拨:知识:变量控制,氧化还原反应规律,反应速率的计算,实验假设及实验方案的设计。能力:考查将分析问题的过程和结论用正确的语言作出解释的能力,以及初步进行化学实验研究的一般过程,实验分析、设计以及探究能力。试题难度:较大。


科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 有机化学基础练习卷(解析版) 题型:填空题
已知:

水杨酸E为紫外线吸收剂,可用于配制防晒霜。E的一种合成路线如下:

请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%,则A的分子式为________;结构分析显示A只有一个甲基,A的名称为________。
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为__________________________。
(3)C有________种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂:________。
(4)第③步的反应类型为________;D所含官能团的名称为________。
(5)写出同时符合下列条件的水杨酸所有同分异构体的结构简式:__________________________。
a.分子中有6个碳原子在一条直线上;
b.分子中所含官能团包括水杨酸具有的官能团。
(6)第④步的反应条件为________;写出E的结构简式:______________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学能与热能练习卷(解析版) 题型:选择题
向足量H2SO4溶液中加入110 mL 0.4 mol/L Ba(OH)2溶液,放出的热量是5.12 kJ。如果向足量Ba(OH)2溶液中加入110 mL 0.4 mol/L HCl溶液时,放出的热量是2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为( )
A.Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH=-0.72 kJ/mol
B.Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH=-2.92 kJ/mol
C.Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH=-16.4 kJ/mol
D.Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH=-73.0 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学实验基础练习卷(解析版) 题型:选择题
下列实验操作与预期实验目的或实验结论不一致的是( )
选项实验操作及现象实验目的或结论
A用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色可证明氧化性:H2O2比Fe3+强
B在0.1 mol/L的NaHCO3溶液中,加2滴酚酞显浅红色,微热,溶液颜色加深 验证盐类水解反应是吸热反应
C将一定量的NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤 得到NaCl晶体
D苯酚钠溶液中通入足量二氧化碳产生浑浊苯酚的酸性弱于碳酸
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学实验基础练习卷(解析版) 题型:选择题
下列实验现象及相关结论均正确的是( )
ABCD
实验



现象品红褪色最后试管有浅黄色沉淀最后一滴标准液使酚酞由无色变为红色,且30s内不复原 盐桥左端从无色逐渐变为蓝色
结论SO2有
强氧化性有机物中含有溴原子滴定达到终点金属Ⅱ比Ⅰ活泼
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学基本理论练习卷(解析版) 题型:选择题
常温下,对下列电解质溶液的有关说法正确的是( )
A.相同浓度和体积的强碱和强酸溶液混合后,溶液的pH一定等于7
B.在NaHCO3溶液中,c(CO32—)>c(HCO3—)
C.在有AgCl沉淀的溶液中加入NaCl固体,c(Ag+)减小
D.将pH相等的CH3COONa和Na2CO3溶液稀释相同倍数,CH3COONa溶液的pH较大
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学基本理论练习卷(解析版) 题型:选择题
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )

A.0.1 mol CuO B.0.1 mol CuCO3
C.0.1 mol Cu(OH)2 D.0.05 mol Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 化学基本概念练习卷(解析版) 题型:选择题
运用有关概念判断下列叙述正确的是( )
A.1 mol H2燃烧放出的热量为H2的燃烧热
B.Na2SO3与H2O2的反应为氧化还原反应
C. 和
和 互为同系物
互为同系物
D.BaSO4的水溶液不易导电,故BaSO4是弱电解质
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习必做训练 元素及其化合物练习卷(解析版) 题型:填空题
合金是建造航空母舰的主体材料。
(1)航母升降机可由铝合金制造。
①铝元素在周期表中的位置为________。工业炼铝的原料由铝土矿提取而得,提取过程中通入的气体为________。
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为____________________________________。
焊接过程中使用的保护气为________(填化学式)。
(2)航母舰体材料为合金钢。
①舰体在海水中发生的电化学腐蚀主要为________。
②航母用钢可由低硅生铁冶炼而成,则在炼铁过程中为降低硅含量需加入的物质为________。
(3)航母螺旋桨主要用铜合金制造。
①80.0 g Cu-Al合金用酸完全溶解后,加入过量氨水,过滤得白色沉淀39.0 g,则合金中Cu的质量分数为________。
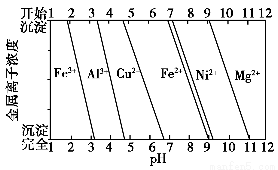
②为分析某铜合金的成分,用酸将其完全溶解后,用NaOH溶液调节pH,当pH=3.4时开始出现沉淀,分别在pH为7.0、8.0时过滤沉淀,结合题图信息推断该合金中除铜外一定含有________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com