
【题目】元素铬(Cr)在自然界主要以+3价和+6价存在。请回答下列问题:
(1)+6价的Cr能引起细胞的突变而对人体不利,可用 Na2SO3 将Cr2O72—还原为Cr3+。该反应的离子反应方程式为___________。
(2)利用铬铁矿(FeOCr2O3)冶炼制取金属铬的工艺流程如图所示:

①为加快焙烧速率和提高原料的利用率,可采取的措施之一是__________________________ 。
②“水浸”要获得浸出液的操作是_________________________________。浸出液的主要成分为Na2CrO4,向“滤液”中加入酸化的氯化钡溶液有白色沉淀生成,则 “还原”操作中发生反应的离子方程式为___。
③加热Cr(OH)3可得到Cr2O3,从工业成本角度考虑,用Cr2O3制取金属Cr的冶炼方法是 _______。
(3)已知 Cr3+完全沉淀时溶液pH为5,(Cr3+浓度降至10-5molL-1可认为完全沉淀)则Cr(OH)3的溶度积常数 Ksp=_______________。
(4)用石墨电极电解铬酸钠(Na2CrO4)溶液,可制重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2Cr![]() +2H+
+2H+![]() Cr2
Cr2![]() + H2O)。
+ H2O)。
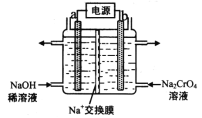
①电极b连接电源的______极(填“正”或“负”) , b 极发生的电极反应式为_________________。
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol,则理论上生成重铬酸钠的物质的量是 _______________mol 。
【答案】Cr2O72—+3SO32-+8H+=2Cr3++3SO42-+4H2O 铬铁矿粉碎 过滤 8CrO42—+3S2-+20H2O=8Cr(OH)3↓+3SO42-+16OH- CO高温还原Cr2O3(热还原法) 1×10-32 正 2H2O-4e-=O2↑+4H+ ![]()
【解析】
(1)分析元素化合价变化情况,依据得失电子守恒,原子个数守恒,得出离子反应方程式。
(2)①影响化学反应速率的因素:物质的表面积大小,表面积越大,反应速率越快。
②依据原子守恒和得失电子守恒,得出离子方程式。
③用Cr2O3制取金属Cr,可以采取CO高温还原Cr2O3(热还原法)。
(3)根据Ksp=c(Cr3+)c3(OH-)求算。
(4)①根据装置图和离子放电顺序得出阳极的电极反应式。
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol,则溶液中移动的电荷为(a-b)mol,所以外电路转移的电子为(a-b)mol,阳极的电极反应为2H2O-4e-=O2↑+4H+,则阳极生成的氢离子为(a-b)mol。
(1)反应中铬元素化合价从+6价降为+3价,硫元素从+4价升高到+6价,依据得失电子守恒,原子个数守恒,离子反应方程式为Cr2O72—+3SO32-+8H+=2Cr3++3SO42-+4H2O,故答案为:Cr2O72—+3SO32-+8H+=2Cr3++3SO42-+4H2O。
(2)①影响化学反应速率的因素:物质的表面积大小,表面积越大,反应速率越快,为加快焙烧速率和提高原料的利用率,可采取的措施将铬铁矿粉碎,故答案为:铬铁矿粉碎。
②“水浸”要获得浸出液,要过滤出浸渣,采取的操作是过滤;浸出液的主要成分为Na2CrO4,向“滤液”中加入酸化的氯化钡溶液有白色沉淀生成,说明加入的Na2S被氧化成SO42-,Cr元素由+6价降为+3价,S元素由-2价升到+6价,依据原子守恒和得失电子守恒,得到反应为:8CrO42—+3S2-+20H2O=8Cr(OH)3↓+3SO42-+16OH-,故答案为:过滤;8CrO42—+3S2-+20H2O=8Cr(OH)3↓+3SO42-+16OH-。
③从工业成本角度考虑,用Cr2O3制取金属Cr,可以采取CO高温还原Cr2O3(热还原法),故答案为:CO高温还原Cr2O3(热还原法)。
(3)pH为5,c(OH-)=10-9,Ksp=c(Cr3+)c3(OH-)=10-5×(10-9)3=1×10-32,故答案为:1×10-32。
(4)①根据图示,在b极所在电极室得到Na2Cr2O7,根据2CrO42-+2H+![]() Cr2O72—+ H2O ,电解过程中b极c(H+)增大,则b极电极反应式为2H2O-4e-=O2↑+4H+,a是阴极,b是阳极,电极b连接电源的正极,故答案为:正;2H2O-4e-=O2↑+4H+。
Cr2O72—+ H2O ,电解过程中b极c(H+)增大,则b极电极反应式为2H2O-4e-=O2↑+4H+,a是阴极,b是阳极,电极b连接电源的正极,故答案为:正;2H2O-4e-=O2↑+4H+。
②电解一段时间后,测得阳极区溶液中Na+物质的量由a mol变为b mol,则溶液中移动的电荷为(a-b)mol,阴极电极反应式为2H2O+2e-=H2↑+2OH-,则电路中通过电子物质的量为(a-b)mol;阳极的电极反应式为2H2O-4e-=O2↑+4H+,则阳极生成的氢离子为(a-b)mol,结合2CrO42-+2H+![]() Cr2O72—+ H2O,所以阳极生成的Cr2O72—物质的量是
Cr2O72—+ H2O,所以阳极生成的Cr2O72—物质的量是![]() mol,故答案为:
mol,故答案为:。


科目:高中化学 来源: 题型:
【题目】降冰片二烯类化合物是一类太阳能储能材料。降冰片二烯在紫外线照射下可以发生下列转化。下列说法错误的是( )
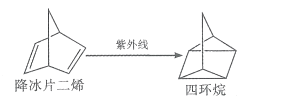
A. 降冰片二烯与四环烷互为同分异构体
B. 降冰片二烯能使酸性高锰酸钾溶液褪色
C. 四环烷的一氯代物超过三种(不考虑立体异构)
D. 降冰片二烯分子中位于同一平面的碳原子不超过4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年研究表明离子液体型催化剂GIL可对某些特定加成反应有很好的催化作用,有机化合物H的合成路线如下:
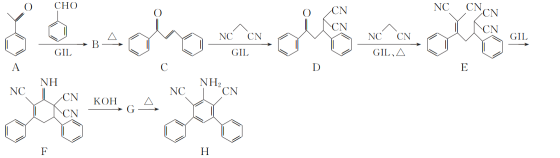
(1)C中含有的官能团名称为_____。
(2)C→D的反应类型为_____。
(3)已知:G和H的分子式相同,F→G和B→C反应类型也相同,那么G的结构简式为_____。
(4)写出满足下列条件的B的一种同分异构体X的结构简式:_____。
①1molX完全水解消耗2molNaOH;
②水解酸化后两种产物核磁共振氢谱均有4个峰,峰高比为3∶2∶2∶1。
(5)以乙醇为原料利用GIL合成聚酯![]() 写出合成路线流程图(无机试剂可任选,合成路线流程图示例见本题题干)。______
写出合成路线流程图(无机试剂可任选,合成路线流程图示例见本题题干)。______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M、N、X、Y四种主族元素在周期表里的相对位置如下图所示,已知它们的原子序数总和为46。

(1)M与Y形成的化合物中含________键,属__________分子。(填“极性”或“非极性”)
(2)N元素形成的单质分子中的化学键类型及数目是__________________(填“σ键”或“π键”)。在化学反应中________易断裂。
(3)由N、Y的氢化物相互作用所生成的物质的电子式为_________________。其中的化学键有__________________________。
(4)写出M单质与X元素最高价氧化物对应的水化物反应的化学方程式_____________。
(5)核电荷数比X元素少8的元素可形成多种粒子,按要求填入空格中:
质子数 | 16 | 16 | 16 |
电子数 | 16 | 17 | 18 |
化学式 | _______ | ________ | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知A、B、C、D四种分子所含原子的数目依次为1、3、6、6,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1∶2。D是一种有毒的有机物。
(1)组成A分子的原子的元素符号是________。
(2)从B分子的立体结构判断,该分子属于________分子(填“极性”或“非极性”)。
(3)C分子中都包含________个σ键,________个π键。
(4)D的熔、沸点比C2H6的熔、沸点高,其主要原因是(需指明D是何物质):________。
Ⅱ.CO的结构可表示为CO,N2的结构可表示为NN。
(5)下表是两者的键能数据:(单位:kJ·mol-1)

结合数据说明CO比N2活泼的原因: ____________________。
Ⅲ.Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关。
(6)基态Ni原子的核外电子排布式为________,基态Cu原子的价电子排布式为________。
(7)Fe(CO)5常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于________(填晶体类型)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究处理NOx、SO2,对环境保护有着重要的意义。回答下列问题:
(1)SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。已知吸收过程中相关反应的热化学方程式如下:① SO2(g) + NH3H2O(aq) =NH4HSO3(aq) △H1 = a kJmol-1;② NH3H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq) + H2O(l)△H2 = b kJmol-1;③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq) △H3= c kJmol-1,则反应 2SO2(g) + 4NH3H2O(aq) + O2(g) =2(NH4)2SO4(aq) + 2H2O(l) △H = ______。
(2)NOx的排放主要来自于汽车尾气,有人利用反应C (s) + 2NO(g)![]() N2(g) + CO2(g) △H=-34.0 kJmol-1,用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示:
N2(g) + CO2(g) △H=-34.0 kJmol-1,用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示:
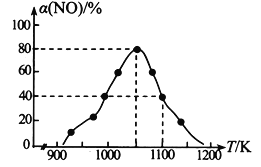
①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是_________________________; 在1100K 时,CO2的体积分数为______。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa 时,该反应的化学平衡常数Kp=________(已知:气体分压=气体总压×体积分数)。
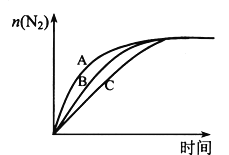
(3)在高效催化剂的作用下用CH4还原NO2,也可消除氮氧化物的污染。在相同条件下,选用A、B、C三种不同催化剂进行反应,生成 N2的物质的量与时间变化关系如图所示,其中活化能最小的是_________(填字母标号)。
(4)在汽车尾气的净化装置中 CO和NO发生反应:2NO(g) + 2CO(g)![]() N2(g) + 2CO2(g) △H2 =-746.8 kJmol-1。实验测得,υ正=k正c2(NO) c2(CO) ,υ逆=k逆c(N2) c2(CO2) (k正、k逆为速率常数,只与温度有关)。
N2(g) + 2CO2(g) △H2 =-746.8 kJmol-1。实验测得,υ正=k正c2(NO) c2(CO) ,υ逆=k逆c(N2) c2(CO2) (k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数_____(填" >”、“< ”或“=”) k逆增大的倍数。
②若在1L 的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则![]() =_____(保留2位有效数字)。
=_____(保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,N表示粒子数。下列叙述正确的是( )
A. 在标准状况下2.24LCCl4中含有的C—Cl键数为0.4NA
B. 将1mol Cl2通入水中,则N(HClO)+N(Cl)+N(ClO)=2NA
C. 将CO2通过Na2O2使其质量增加a g时,反应转移的电子数为aNA/14
D. 3.0g含甲醛(HCHO)的冰醋酸中含有的原子总数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 | H2C2O 4 | K1=5.4×10-2 K2=5.4×10-5 | H2S | K1=1.3×10-7 K2=7.1×10-15 |
HClO | 3×10-8 |
请回答下列问题:
(1)同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是__________。
(2)常温下0.1 molL-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是_______(填序号)。
A.c(H+) B. c(H+)/c(CH3COOH) C. c(H+)/c(OH-) D. c(OH-)
(3)0.1 molL-1的H2C2O4溶液与0.1 molL-1的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为______________。
(4)pH相同的NaClO和CH3COOK溶液,其溶液的物质的最浓度的大小关系是:CH3COONa______NaClO,两溶液中:[c(Na+)-c(ClO-)]______[c(K+)-c(CH3COO-)](填“>”“<”或“=”)。
(5)向0.1 molL-1CH3COOH 溶液中滴加 NaOH 溶液至 c(CH3COOH): c(CH3COO-)=5 : 9,此时溶液pH=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 所含共价键数均为0.4NA的白磷(P4)和甲烷的物质的量相等
B. 1 mol Na与O2反应,生成Na2O和Na2O2的混合物共失去NA个电子
C. 1mol Na2O2固体中含有离子总数为4NA
D. 25℃时,pH=13的氢氧化钠溶液中约含有NA个氢氧根离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com