
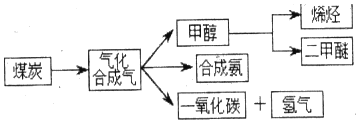
分析 化学平衡常数指在一定温度下,可逆反应达到平衡时,各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写方程式.
解答 解:平衡表达式为:K=$\frac{c({H}_{2})•c(CO)}{c({H}_{2}O)}$,生成物为CO、H2,反应物含有H2O,三者化学计量数分别为1、1、1,根据元素守恒,故另一反应物为固体C,反应中它所对应反应的化学方程式为C(s)+H2O(g)?CO(g)+H2(g),故答案为:C(s)+H2O(g)?CO(g)+H2(g).
点评 本题考查化学平衡常数来书写化学方程式,难度中等,判断有固体碳参加反应是关键.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯可以使溴水褪色 | |
| B. | 乙烷与氯气发生取代反应,产物共有7种 | |
| C. | 煤中含有苯、甲苯和二甲苯 | |
| D. | 乙酸和油脂都能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
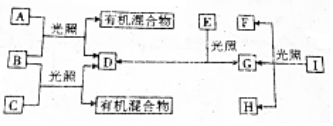
 ,有机物C的结构简式为
,有机物C的结构简式为 ,其苯环上的二氯代物共有6种.
,其苯环上的二氯代物共有6种.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
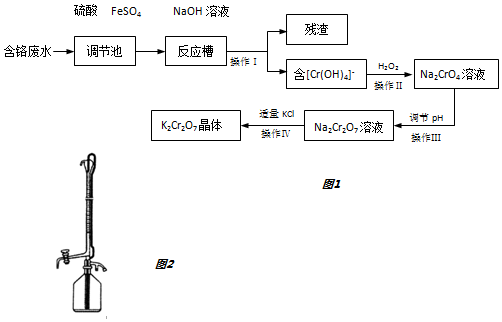
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯碱工业中电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| B. | 氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ | |
| C. | 氢氧化钠溶液吸收少量二氧化硫SO2+OH-=HSO3- | |
| D. | 稀硫酸中加氢氧化钡溶液至中性:Ba2++H++OH-+SO42-=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 救灾用的葡萄糖溶液能产生丁达尔效应 | |
| B. | 福尔马林可用于洪水后环境消毒和鱼肉等食益的防腐保鲜 | |
| C. | 医用酒精可用于灾后饮用水消毒 | |
| D. | 淀粉、油脂、蛋白质可为灾民提供营养 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
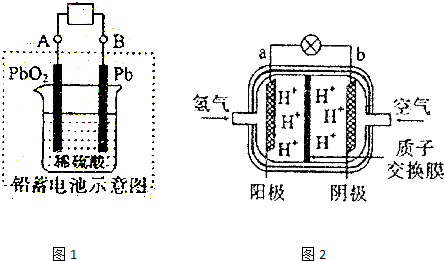
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com