
设NA表示阿伏加德罗常数,下列叙述中正确的是()
A. 常温常压下,11.2L氧气所含的原子数为NA
B. 在常温常压下,22g二氧化碳中含有的原子数为1.5 NA
C. 在标准状况下,5.6L四氯化碳含有的分子数为0.25NA
D. 在非标准状况下,22.4LO2含有的分子数一定不是NA
考点: 阿伏加德罗常数.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A、气体摩尔体积vm=22.4L/mol使用条件是标准状况(0°C,101kPa);
B、二氧化碳分子中含有3个原子,22g二氧化碳的物质的量为0.5mol,含有1.5mol原子;
C、标况下,四氯化碳是液态;
D、非标准状况下,气体摩尔体积也可能是22.4L/mol.
解答: 解:A、不是标准状况,不能使用气体摩尔体积vm=22.4L/mol,11.2L氧气的物质的量不是0.5mol,所含的原子数不是NA,故A错误;
B.22g二氧化碳的物质的量为: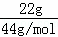 =0.5mol,0.5mol二氧化碳中含有1.5mol原子,含有的原子数为1.5NA,故B正确;
=0.5mol,0.5mol二氧化碳中含有1.5mol原子,含有的原子数为1.5NA,故B正确;
C、标况下,四氯化碳是液态,故C错误;
D、.由PV=nRT可知,在非标准状况下,气体摩尔体积也可能是22.4L/mol,故在非标准状况下,22.4L氧气的物质的量也可能是1mol,分子数也可能是NA个,故D错误;
故选B.
点评: 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
对CH3﹣CH=CH﹣C≡C﹣CF3分子结构的下列叙述中,正确的是( )
|
| A. | 6个碳原子有可能都在同一直线上 |
|
| B. | 在同一直线上的原子至少有5个 |
|
| C. | 在同一平面上的原子至少有8个 |
|
| D. | 分子中呈四面体结构的碳原子有3个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于主族元素电子排布特征的说法正确的是()
A. 主族元素的原子核外电子最后填入的能级是s能级
B. 主族元素的原子核外电子最后填入的能级是s能级或p能级
C. 主族元素的原子核外电子最后填入的能级是d能级或f能级
D. 主族元素的原子核外电子最后填入的能级是s能级或d能级
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下,下列物质占体积最大的是()
A. 0.6 g H2 B. 98 g H2SO4
C. 6.02×1022个CO2 D. 4.48 L HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,Cl﹣的物质的量浓度与50mL 1mol/L AlCl3溶液中Cl﹣物质的量浓度相等是()
A. 100mL 1mol/LNaCl溶液 B. 150mL 3mol/LKCl溶液
C. 75mL 1mol/LMgCl2溶液 D. 25mL 2mol/LAlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下列反应的离子方程式
(1)硫酸氢钠溶液中加入硝酸钡溶液产生白色沉淀: ;
(2)在小苏打(NaHCO3)溶液中加盐酸,有无色气体产生: ;
(3)在200mL的烧杯中加入50mL蒸馏水,加热至沸腾,滴入10滴饱和氯化铁溶液,继续加热至溶液呈红褐色 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关溶液组成的描述合理的是( )
A.无色溶液中可能大量存在Al3+、NH4+、Cl-、S2-
B.酸性溶液中可能大量存在Na+、ClO-、SO42-、I-
C.弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3-
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
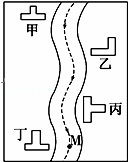
某小河边有四座工厂:甲、乙、丙、丁(如图所示).已知,它们所排出的废液里分别含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某环保小组对河水监测时发现:①甲处河水呈乳白色②乙处河水呈红褐色浑浊状③丙处河水由浑浊变清④丁处河水产生气泡,河水仍澄清.
请推断:
(1)四座工厂排出的废液里含有的污染物是甲 ,乙 ,丙 ,丁 .
在M处取出的河水中,肯定大量存在的离子有 .
(3)用离子方程式表示丙除河水变澄清的原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计及其对应的离子方程式均正确的是()
A. 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+
B. Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH﹣+O2↑
C. 将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl﹣+ClO﹣
D. 用惰性电极电解饱和氯化钠溶液:2Cl﹣+2H+ H2↑+Cl2↑
H2↑+Cl2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com