
| A、少量金属钠保存在煤油里 |
| B、氯水保存在无色透明的试剂瓶中 |
| C、工业上采用电解熔融MgO的方法制备金属Mg |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |


科目:高中化学 来源: 题型:
| A、1mol氯气参加氧化还原反应时电子转移2NA |
| B、3.2g SO2与2.3g NO2所含有的氧原子数相等 |
| C、1mol Na2O2与足量水反应后转移的电子数为NA |
| D、1L0.1mol/L MgCl2溶液中Cl-离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、24kg | B、68kg |
| C、136kg | D、680kg |
查看答案和解析>>
科目:高中化学 来源: 题型:
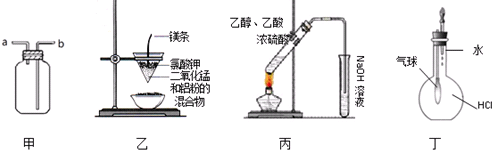
| A、装置甲:气体从a口进入,收集CO2 |
| B、装置乙:可制得金属锰 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:验证HCl气体在水中的溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验 | 操作 |
| A | 钠与水反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 鉴别KCl、NH4Cl和MgCl2溶液 | 分别向三种溶液中滴加NaOH溶液至过量并加热 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、νA=2mol/L?min (正反应速率);νA=2mol/L?min(逆反应速率) |
| B、νA=2mol/L?min(正反应速率);νC=2mol/L?min(逆反应速率) |
| C、νA=1mol/L?min (正反应速率);νB=2mol/L?min(逆反应速率) |
| D、νA=1mol/L?min(正反应速率);νC=1.5mol/L?min(逆反应速率) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com